Thamani za Thermodynamic zinajadiliwa kwa kuzingatia mfumo na mazingira yake. Kila kitu ambacho sio sehemu ya mfumo hufanya mazingira yake. Mfumo na mazingira yanatenganishwa na mpaka. Kwa mfano, ikiwa mfumo ni moja ya gesi katika chombo, basi mpaka ni ukuta wa ndani wa chombo yenyewe. Kila kitu nje ya mpaka kinazingatiwa mazingira, ambayo yangejumuisha kontena yenyewe.
Mpaka lazima uelezwe vizuri, kwa hivyo mtu anaweza kusema wazi ikiwa sehemu fulani ya ulimwengu iko kwenye mfumo au katika mazingira yaliyozunguka. Ikiwa jambo hilo haliwezekani kupitisha mpaka, basi mfumo unasemekana kufungwa; la sivyo, iko wazi. Mfumo uliofungwa bado unaweza kubadilishana nishati na mazingira isipokuwa mfumo huo ni wa pekee, kwa hali ambayo haijalishi na nguvu haziwezi kupita mpaka.
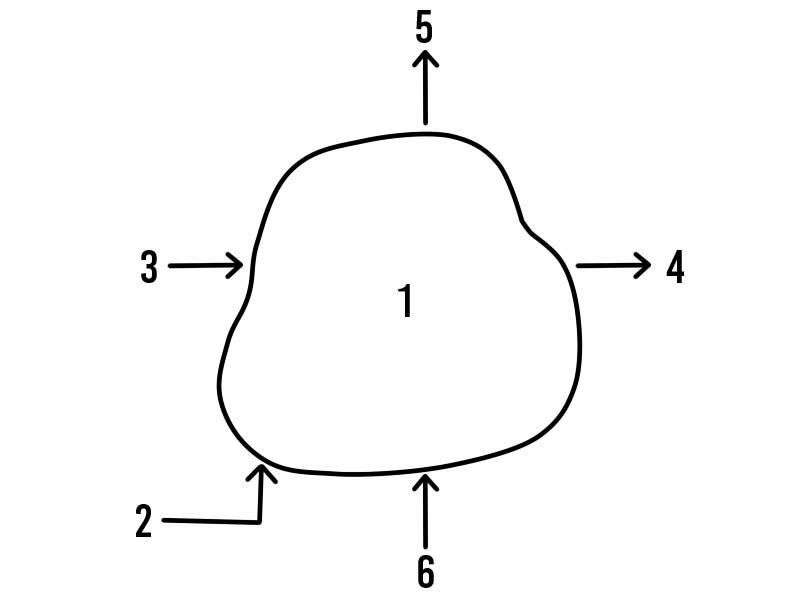
Sheria ya kwanza ya thermodynamics, pia inajulikana kama Sheria ya Uhifadhi wa Nishati, inasema kwamba nishati haiwezi kuunda au kuharibiwa; nishati inaweza kuhamishwa au kubadilishwa kutoka fomu moja kwenda nyingine. Kwa mfano, kuwasha taa kungeonekana kutoa nguvu; Walakini, ni nishati ya umeme ambayo inabadilishwa.
Njia ya kuelezea sheria ya kwanza ya thermodynamics ni kwamba mabadiliko yoyote katika nishati ya ndani (∆E) ya mfumo hupewa na jumla ya joto (q) ambayo inapita mipaka yake na kazi (w) iliyofanywa kwenye mfumo na mazingira.
∆E = q + w
ambapo q ni joto ambalo linapita kati ya mipaka yake na w ni kazi iliyofanywa kwenye mfumo na mazingira
Sheria hii inasema kuwa kuna aina mbili za michakato, joto, na kazi, ambayo inaweza kusababisha badiliko katika nishati ya ndani ya mfumo. Kwa kuwa joto na kazi zinaweza kupimwa na kuainishwa, hii ni sawa na kusema kuwa mabadiliko yoyote katika nishati ya mfumo lazima yatoleta mabadiliko yanayofanana katika nishati ya mazingira ya nje ya mfumo. Kwa maneno mengine, nishati haiwezi kuunda au kuharibiwa. Ikiwa joto linapita ndani ya mfumo au mazingira hufanya kazi juu yake, nishati ya ndani huongezeka na ishara ya q na w ni chanya. Kinyume chake, mtiririko wa joto nje ya mfumo au kazi iliyofanywa na mfumo (kwenye mazingira) itakuwa kwa gharama ya nishati ya ndani, na q na w, kwa hivyo, itakuwa hasi.
Sheria ya pili ya thermodynamics inasema kwamba entropy ya mfumo wa pekee huongezeka kila wakati. Mifumo ya kutengwa inabadilika kwa hiari kuelekea usawa wa mafuta - hali ya upeo mkubwa wa mfumo. Kwa ufupi, kuingia kwa ulimwengu (mfumo wa pekee wa pekee) huongezeka tu na kamwe hupungua.
Njia rahisi ya kufikiria sheria ya pili ya thermodynamics ni kwamba chumba, ikiwa hakijasafishwa na kuoshwa, mara kwa mara kitakuwa cha fujo na hasi kwa wakati - bila kujali mtu ni mwangalifu sana kuiweka safi. Wakati chumba kinasafishwa, kuingia kwake kunapungua, lakini juhudi ya kuisafisha imesababisha kuongezeka kwa entropy nje ya chumba ambacho kinazidi entropy iliyopotea.
Sheria ya tatu ya thermodynamics inasema kwamba entropy ya mfumo inakaribia thamani ya mara kwa mara wakati joto linakaribia sifuri kabisa. Entropy ya mfumo katika sifuri kabisa ni kawaida sifuri, na katika hali zote imedhamiriwa tu na idadi ya majimbo tofauti ambayo ina. Hasa, entropy ya dutu safi ya fuwele (utaratibu kamili) kwa joto kabisa la sifuri ni sifuri. Taarifa hii inashikilia kuwa kweli ikiwa kioo kamili ina serikali moja tu na nguvu ya chini.