Химийн элементүүдийн үечилсэн хүснэгт нь мэдэгдэж буй элементүүдийн жагсаалт юм. Хүснэгтэнд элементүүдийг хамгийн бага тооноос эхлэн атомын дугаарын дарааллаар байрлуулна. Элементийн атомын дугаар нь тухайн атом дахь протоны тоотой ижил байна.
Дмитрий Менделеев орчин үеийн үелэх системийг зохион бүтээсэн гавьяатай.
Элемент бүр үелэх системд квадраттай байдаг. Талбай бүрт 3 мэдээлэл байна
- элементийн нэр
- түүний албан ёсны химийн тэмдэг
- түүний атомын дугаар
Жишээлбэл, төмрийн квадрат нь иймэрхүү харагдах болно.
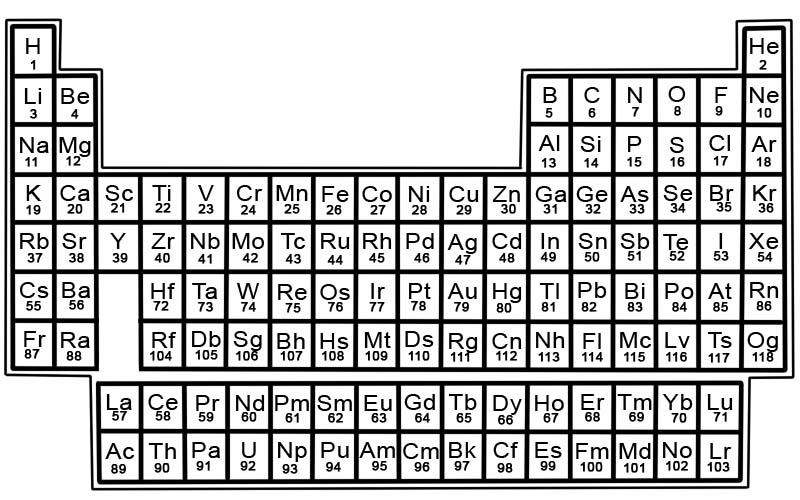
Тогтмол системийн элементүүдийг мөр, багананд байрлуулна.
- Мөрүүдийг үе гэж нэрлэдэг. Үе үе гэдэг нь шинж чанар нь аажмаар, урьдчилан таамаглахуйц өөрчлөгддөг үелэх систем дэх элементүүдийн эгнээ юм.
- Багануудыг бүлгүүд гэж нэрлэдэг. Тогтмол систем нь 18 баганатай. Багана бүр элементийн бүлэг буюу гэр бүлийг агуулна. Бүлэг нь ижил төстэй физик эсвэл химийн шинж чанартай элементүүдийг агуулдаг.
Тогтмол хүснэгт дээрх бүсүүд
Тогтмол хүснэгтийг хэсэг болгон хувааж болно.
Нэг хэсэг нь эхний хоёр бүлэг буюу 1, 2-р бүлэг, 3-18-р бүлгийн элементүүдээс бүрдэнэ. Эдгээр нь төлөөлөх элементүүд юм. Эдгээрт металл, металлоид, металл бус зэрэг орно.
Металл
Жишээ нь: төмөр, цагаан тугалга, натри, плутони.
- өрөөний температурт ихэвчлэн хатуу (мөнгөн ус үл хамаарах зүйл)
- өндөр гялбаа (гялалзсан)
- металл төрх
- дулаан, цахилгаан сайн дамжуулагч
- уян хатан (нимгэн хуудас болгон нугалж, нугалж болно)
- уян хатан (утасанд татах боломжтой)
- агаар, далайн усанд зэврэх буюу исэлдүүлэх
- ихэвчлэн нягт (үл хамаарах зүйлд лити, кали, натри орно)
- маш өндөр хайлах цэгтэй байж болно
- электроноо амархан алддаг
Металлоидууд
Жишээ нь: бор, цахиур, хүнцэл.
- уйтгартай эсвэл гялалзсан
- ихэвчлэн дулаан, цахилгаан дамжуулдаг, гэхдээ метал шиг сайн биш
- ихэвчлэн сайн хагас дамжуулагч хийдэг
- ихэвчлэн хэд хэдэн хэлбэрээр байдаг
- ихэвчлэн уян хатан байдаг
- ихэвчлэн уян хатан байдаг
- урвалын явцад электрон олж авах эсвэл алдаж болно
Төмөр бус
Жишээ нь: хүчилтөрөгч, хлор, аргон.
- уйтгартай дүр төрх
- ихэвчлэн хэврэг байдаг
- дулаан, цахилгаан дамжуулагч муу
- металлтай харьцуулахад ихэвчлэн бага нягттай байдаг
- металлтай харьцуулахад ихэвчлэн хатуу бодисын хайлах цэг бага байдаг
- химийн урвалын явцад электрон авах хандлагатай байдаг
1 ба 2-р бүлэг
- 1-р бүлэг - Шүлтлэг металлууд. Жишээ нь: натри, лити, кали.
- 2-р бүлэг - Шүлтлэг шороон металл Жишээ нь: бериллий, магни, кальци, бари, радий. Шүлтлэг шороон металл бүр нь ижил хугацаанд шүлтлэг металлаас илүү нягт, хатуу бөгөөд хайлах цэг нь өндөр байдаг. Шүлтлэг шороон металууд нь реактив боловч шүлтлэг метал шиг урвалд ордоггүй.
13-18 бүлэг
13-р бүлэг - Борын гэр бүл
- Жишээ нь: бор (B), хөнгөн цагаан (Al), галли (Ga), индий (In), талли (Tl).
- Тэд гурван валентийн электронтой.
14-р бүлэг - Нүүрстөрөгчийн гэр бүл
- Жишээ нь: нүүрстөрөгч (C), цахиур (Si), германий (Ge), цагаан тугалга (Sn), хар тугалга (Pb).
- Тэд бүгд дөрвөн валентийн электронтой.
15-р бүлэг - Азотын гэр бүл
- Жишээ нь: азот (N), фосфор (P), хүнцэл (As), сурьма (Sb), висмут (Bi).
- Эдгээр элементүүд бүгд таван валентийн электронтой.
- Азот ба фосфор нь металл биш юм.
16-р бүлэг - Хүчилтөрөгчийн гэр бүл
- Жишээ нь: хүчилтөрөгч (O), хүхэр (S), селен (Se), теллур (Te), цацраг идэвхт полони (Po).
- Энэ бүлэг нь зургаан валентийн электронтой
- Эдгээрийг халькоген гэж бас нэрлэдэг.
17-р бүлэг - Галоген
- Жишээ нь: фтор (F), хлор (Cl), бром (Br), иод (I), астатин (At).
- Тэд долоон валентийн электронтой.
- Энэ бүлэг нь бүхэлдээ металл бусаас бүрддэг анхны бүлэг юм.
- Галогенүүд нь өндөр урвалд ордог тул хангалттай хэмжээгээр биологийн организмд хортой эсвэл үхэлд хүргэдэг.
- X тэмдгийг ихэвчлэн аливаа галогенийг илэрхийлэхэд ашигладаг.
- "Галоген" гэдэг нэр нь "давс үүсгэдэг" гэсэн утгатай. Галоген нь металлуудтай урвалд ороход кальци, фтор, натрийн хлорид (хүснэгтийн давс), мөнгөний бромид, калийн иодид зэрэг олон төрлийн давс үүсгэдэг.
18-р бүлэг - Сайн хий
- Гели, неон, аргон, криптон, ксенон, радон гэсэн зургаан сайхан хий байдаг.
- Эдгээр нь бүгд хий бөгөөд агаарт байдаг. Тэд агаар мандлын 0.96 орчим хувийг эзэлдэг.
- Тэд бүгд моноатом бөгөөд молекул бүр нь нэг атом гэсэн үг.
- Тэд бусад элементүүдтэй бараг хэзээ ч урвалд ордоггүй. Учир нь тэдгээр нь бүтэн 8 электрон гадаад электрон бүрхүүлтэй байдаг.
- Эрхэмсэг хий нь маш бага буцлах, хайлах цэгтэй тул тэдгээрийг криоген хөргөлтийн бодис болгон ашигладаг.
Шилжилтийн металлууд
- 3-12-р бүлгийн элементүүд нь шилжилтийн элементүүд юм.
- Тэд бүгд металл юм.
- Ихэнх шилжилтийн элементүүд нь хүдэрт бусад элементүүдтэй хавсарсан байдаг.
- Алт, мөнгө гэх мэт цөөн хэдэн шилжилтийн элементүүд нь цэвэр элемент юм.
- Гэрлийн чийдэнгийн утаснууд нь гянтболдоор хийгдсэн (элемент 74) нь ямар ч металлаас хамгийн өндөр хайлах цэгтэй бөгөөд гүйдэл дамжин өнгөрөхөд хайлдаггүй.
- Металлуудаас хамгийн бага хайлах цэгтэй мөнгөн усыг термометр, барометрт ашигладаг.
- Мөнгөн ус бол өрөөний температурт шингэн байдаг цорын ганц металл юм.
Төмөр гурвалсан
4-р бүлгийн гурван элемент болох төмөр, кобальт, никель нь ижил төстэй шинж чанартай тул тэдгээрийг төмрийн гурвал гэж нэрлэдэг.
Платинум бүлэг
Рутени, родий, палладий, осми, иридиум, цагаан алт зэрэг нь ижил төстэй шинж чанартай байдаг тул заримдаа цагаан алтны бүлэг гэж нэрлэдэг. Тэд бусад элементүүдтэй амархан нийлдэггүй. Үүний үр дүнд тэдгээрийг катализатор болгон ашиглаж болно.
Дотоод шилжилтийн элементүүд
Дотоод шилжилтийн элементүүд гэж нэрлэгддэг зарим шилжилтийн элементүүдийг үндсэн хүснэгтийн доор байрлуулна. Эдгээр элементүүдийг лантанид ба актинидын цуваа гэж нэрлэдэг тул нэг цуврал нь лантан элемент 57, нөгөө цуврал нь актиниум 89 элементийг дагадаг.
Лантанидууд - Церийээс лютети хүртэлх эхний цувралыг лантанидууд гэж нэрлэдэг. Лантанидыг мөн ховор шороо гэж нэрлэдэг байсан, учир нь тэд нэгэн цагт ховор байдаг гэж үздэг. Эдгээр нь хутгаар зүсэж болох зөөлөн металл юм.
Актинидууд - Бүх актинид нь цацраг идэвхт бодис юм. Тори, протактин, уран нь одоо дэлхий дээр байгалиас олдсон цорын ганц актинид юм. Бусад бүх актинидууд нь синтетик элементүүд юм. Синтетик элементүүдийг лаборатори, цөмийн реакторт хийдэг.
