Objetivos de aprendizaje
En esta lección, los estudiantes
- Describir la osmosis y la presión osmótica.
- Describir solvente y soluto
- Describir la solución y los diferentes tipos de solución.
- Comprender el efecto de la ósmosis en las células vegetales.
- Comprender el efecto de la ósmosis en las células animales.
¿Qué es la ósmosis?
La ósmosis es el movimiento del agua desde una alta concentración a una baja concentración a través de una membrana semipermeable. La ósmosis se refiere al movimiento de las moléculas de agua solamente. Es un tipo especial de difusión.
Es un transporte pasivo, lo que significa que no requiere energía para ser aplicado.
Una solución diluida contiene una alta concentración de moléculas de agua, mientras que una solución concentrada contiene una baja concentración de moléculas de agua.
Las diferentes concentraciones de solutos en los dos lados de la membrana causan presión osmótica. Cuando ocurre la ósmosis, el agua se mueve desde el lado de la membrana con una menor cantidad de presión osmótica al lado de la membrana con la mayor cantidad de presión osmótica.
Cuando la concentración de agua es la misma en ambos lados de la membrana, el movimiento del agua molecular será el mismo en ambas direcciones. No habrá movimiento neto de moléculas de agua.
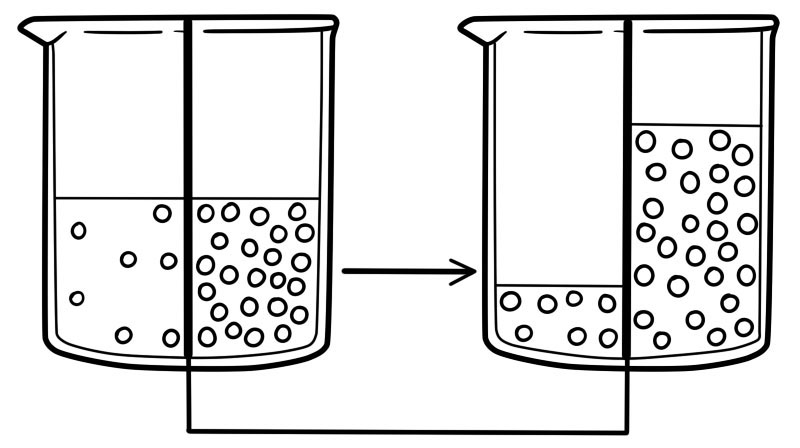
Osmosis a través de células vivas
Las células contienen soluciones diluidas de iones, azúcares y aminoácidos.
La membrana celular es parcialmente permeable. El agua entrará y saldrá de las células por ósmosis.
Un ejemplo importante de ósmosis es el movimiento de moléculas líquidas (solventes) a través de una membrana celular hacia una célula con una mayor concentración de soluto.
¿Qué es la presión osmótica?
La presión osmótica es la presión que causa la difusión del agua a través de membranas semipermeables. Aumenta debido a un aumento en la concentración de solutos en la solución.
¿Qué son los solventes y solutos?
La ósmosis trata con soluciones químicas. Las soluciones tienen dos partes: un solvente y un soluto.
Cuando un soluto se disuelve en un solvente, el producto final se llama solución. El agua salada es un ejemplo de solución; la sal es el soluto y el agua es el solvente.
¿Cuáles son los diferentes tipos de soluciones?
Existen tres tipos de soluciones de ósmosis: la solución isotónica, la solución hipotónica y la solución hipertónica. Los diferentes tipos de soluciones tienen diferentes impactos en las células debido a la ósmosis.
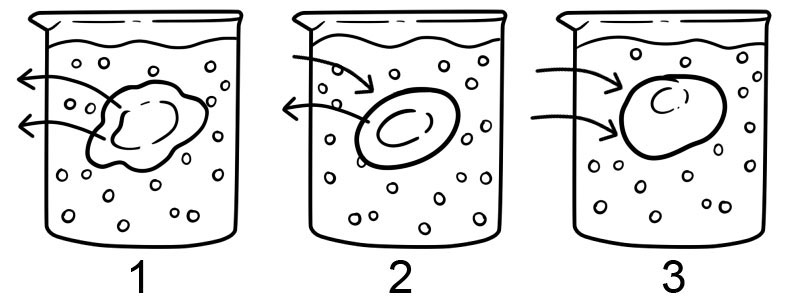
1. Hipertónico : una solución hipertónica es lo opuesto a una solución hipotónica; Hay más soluto fuera de la celda que dentro de ella. En este tipo de solución, el agua sale de la celda y hace que la celda se arrugue.
2. Isotónica : una solución isotónica tiene la misma concentración de solutos tanto dentro como fuera de la célula. En estas condiciones, no hay movimiento neto de solvente; En este caso, la cantidad de agua que entra y sale de la membrana de la célula es igual.
3. Hipotónico : en una solución hipotónica, hay una mayor concentración de solutos dentro de la célula que fuera de la célula. En una solución hipotónica, el agua se mueve hacia la célula y puede hacer que la célula se hinche; Las células que no tienen una pared celular, como las células animales, podrían explotar en este tipo de solución.
Efectos de la ósmosis en las células vegetales.
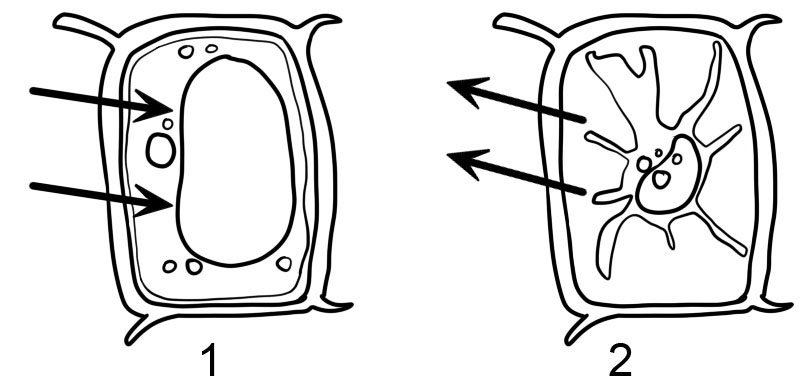
- Hipotónico
- Hipertónico
- Las células vegetales están encerradas por una pared celular rígida. Cuando la célula de la planta se coloca en una solución hipotónica, absorbe agua por ósmosis y comienza a hincharse, pero la pared celular evita que estalle. Se dice que la célula de la planta se ha vuelto 'turgente', es decir, hinchada y dura. La presión dentro de la celda aumenta hasta que esta presión interna es igual a la presión exterior. Esta presión líquida o hidrostática se denomina "presión de turgencia" y evita la mayor entrada neta de agua.
- La turbidez es muy importante para las plantas, ya que ayuda con el mantenimiento de la rigidez y la estabilidad del tejido de la planta, y a medida que cada célula ejerce una presión de turgencia sobre su vecino, crea tensión en el tejido de la planta que permite que las partes verdes de la planta se `` levanten ''. a la luz del sol
- Cuando una célula vegetal se coloca en una solución hipertónica, el agua del interior del citoplasma de la célula se difunde y se dice que la célula vegetal se ha vuelto 'flácida'. Si la célula de la planta se observa bajo un microscopio, se notará que el citoplasma se ha encogido y se ha alejado de la pared celular. Este fenómeno se llama plasmólisis. El proceso se revierte tan pronto como las células se transfieren a una solución hipotónica (deplasmólisis).
- Cuando una célula vegetal se coloca en una solución isotónica, se dice que ocurre un fenómeno llamado "plasmólisis incipiente". 'Incipiente' significa 'a punto de ser'. Aunque la célula no está plasmosificada, tampoco es turgente. Cuando esto sucede, las partes verdes de la planta se caen y no pueden sostener las hojas a la luz del sol.
Efectos de la ósmosis en las células animales.
- Las células animales no tienen paredes celulares, por lo que, en soluciones hipotónicas, las células animales se hinchan y explotan. Si entra demasiada agua en la célula animal, puede explotar, esto se llama lisis. No pueden volverse turgentes porque no hay una pared celular que evite que la célula explote. Cuando la célula está en peligro de explotar, los orgánulos llamados vacuolas contráctiles bombearán agua fuera de la célula para evitar que esto suceda.
- En soluciones hipertónicas, el agua se difunde fuera de la célula debido a la ósmosis y la célula se contrae. Si sale demasiada agua de la célula animal, puede encogerse; esto se llama crenation. Por lo tanto, la célula animal siempre debe estar rodeada de una solución isotónica. En el cuerpo humano, los riñones proporcionan el mecanismo regulador necesario para el plasma sanguíneo. La concentración de agua y sal eliminada de la sangre por los riñones está controlada por una parte del cerebro llamada hipotálamo. El proceso de regulación de la concentración de agua y sales minerales en la sangre se llama osmorregulación.
- Los animales que viven en tierra seca deben conservar agua, al igual que los animales que viven en agua salada. Los animales que viven en agua dulce tienen el problema opuesto; deben deshacerse del exceso de agua tan rápido como entra en sus cuerpos por ósmosis.


