obiettivi formativi
In questa lezione, gli studenti lo faranno
- Descrivere l'osmosi e la pressione osmotica
- Descrivi solvente e soluto
- Descrivere la soluzione e i diversi tipi di soluzione
- Comprendere l'effetto dell'osmosi nelle cellule vegetali
- Comprendere l'effetto dell'osmosi nelle cellule animali
Cos'è l'osmosi?
L'osmosi è il movimento dell'acqua da un'alta concentrazione a una bassa concentrazione attraverso una membrana semipermeabile. L'osmosi si riferisce solo al movimento delle molecole d'acqua. È un tipo speciale di diffusione.
È un trasporto passivo, il che significa che non richiede energia per essere applicato.
Una soluzione diluita contiene un'alta concentrazione di molecole d'acqua, mentre una soluzione concentrata contiene una bassa concentrazione di molecole d'acqua.
Le diverse concentrazioni di soluti sui due lati della membrana causano pressione osmotica. Quando si verifica l'osmosi, l'acqua si sposta dal lato della membrana con una minore quantità di pressione osmotica al lato della membrana con la maggiore quantità di pressione osmotica.
Quando la concentrazione di acqua è la stessa su entrambi i lati della membrana, il movimento molecolare dell'acqua sarà lo stesso in entrambe le direzioni. Non ci sarà alcun movimento netto di molecole d'acqua.
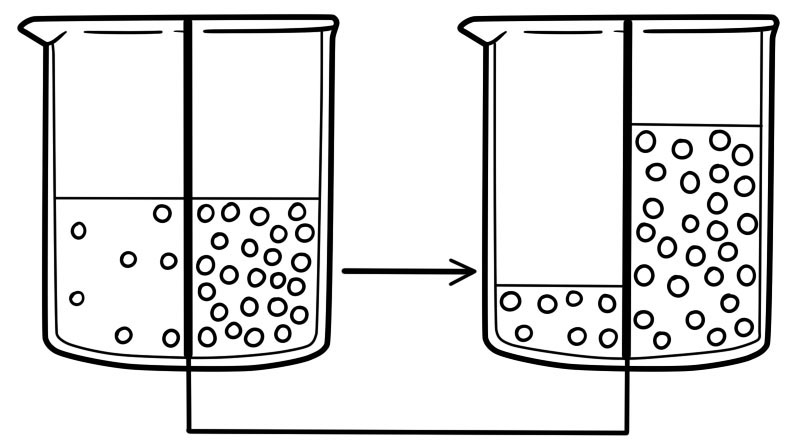
Osmosi tra cellule viventi
Le cellule contengono soluzioni diluite di ioni, zuccheri e amminoacidi.
La membrana cellulare è parzialmente permeabile. L'acqua entra ed esce dalle cellule per osmosi.
Un importante esempio di osmosi è il movimento di molecole liquide (solventi) attraverso una membrana cellulare in una cellula con una concentrazione di soluto più elevata.
Cos'è la pressione osmotica?
La pressione osmotica è la pressione che provoca la diffusione dell'acqua attraverso membrane semipermeabili. Aumenta a causa di un aumento della concentrazione di soluti nella soluzione.
Cosa sono solventi e soluti?
L'osmosi si occupa di soluzioni chimiche. Le soluzioni hanno due parti: un solvente e un soluto.
Quando un soluto si dissolve in un solvente, il prodotto finale è chiamato soluzione. L'acqua salata è un esempio di soluzione; il sale è il soluto e l'acqua è il solvente.
Quali sono i diversi tipi di soluzioni?
Esistono tre tipi di soluzioni di osmosi: la soluzione isotonica, la soluzione ipotonica e la soluzione ipertonica. Diversi tipi di soluzioni hanno impatti diversi sulle cellule a causa dell'osmosi.
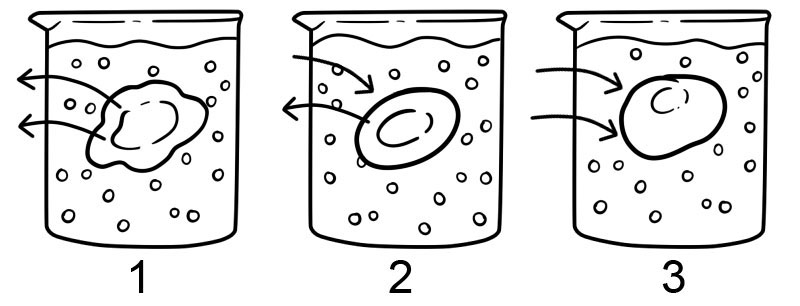
1. Ipertonico - Una soluzione ipertonica è l'opposto di una soluzione ipotonica; c'è più soluto fuori dalla cellula che dentro di essa. In questo tipo di soluzione, l'acqua esce dalla cellula e provoca l'avvizzimento della cellula.
2. Isotonico - Una soluzione isotonica ha la stessa concentrazione di soluti sia all'interno che all'esterno della cellula. In queste condizioni non vi è movimento netto di solvente; in questo caso la quantità di acqua che entra ed esce dalla membrana cellulare è uguale.
3. Ipotonico - In una soluzione ipotonica, c'è una maggiore concentrazione di soluti all'interno della cellula che all'esterno della cellula. In una soluzione ipotonica, l'acqua entra nella cellula e può far gonfiare la cellula; le cellule che non hanno una parete cellulare, come le cellule animali, potrebbero esplodere in questo tipo di soluzione.
Effetti dell'osmosi nelle cellule vegetali
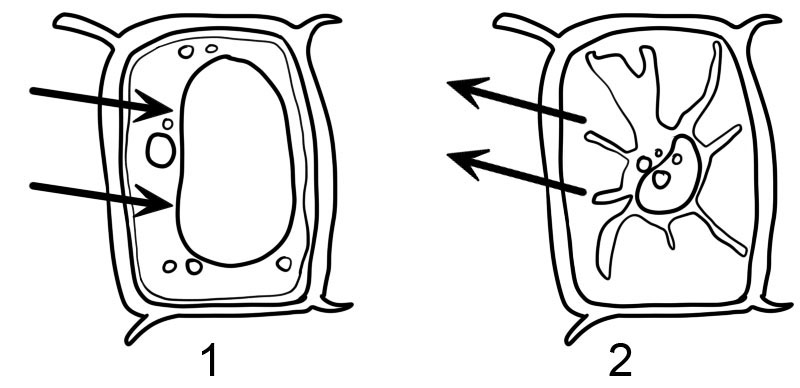
- Ipotonico
- Ipertonico
- Le cellule vegetali sono racchiuse da una parete cellulare rigida. Quando la cellula vegetale viene posta in una soluzione ipotonica, assorbe acqua per osmosi e inizia a gonfiarsi, ma la parete cellulare le impedisce di scoppiare. Si dice che la cellula vegetale sia diventata "turgida", cioè gonfia e dura. La pressione all'interno della cella aumenta fino a quando questa pressione interna è uguale alla pressione esterna. Questa pressione liquida o idrostatica è chiamata "pressione di turgore" e impedisce l'ulteriore apporto netto di acqua.
- Il turgore è molto importante per le piante in quanto aiuta a mantenere la rigidità e la stabilità del tessuto vegetale, e poiché ogni cellula esercita una pressione di turgore sul suo vicino, crea tensione nel tessuto vegetale che consente alle parti verdi della pianta di "alzarsi" alla luce del sole.
- Quando una cellula vegetale viene posta in una soluzione ipertonica, l'acqua dall'interno del citoplasma della cellula si diffonde e si dice che la cellula vegetale sia diventata "flaccida". Se la cellula vegetale viene poi osservata al microscopio, si noterà che il citoplasma si è ritirato e si è allontanato dalla parete cellulare. Questo fenomeno è chiamato plasmolisi. Il processo si inverte non appena le cellule vengono trasferite in una soluzione ipotonica (deplasmolisi).
- Quando una cellula vegetale viene posta in una soluzione isotonica, si verifica un fenomeno chiamato "plasmolisi incipiente". "Incipiente" significa "in procinto di essere". Sebbene la cellula non sia plasmolisata, non è nemmeno turgida. Quando ciò accade, le parti verdi della pianta si abbassano e non sono in grado di sostenere le foglie alla luce del sole.
Effetti dell'osmosi nelle cellule animali
- Le cellule animali non hanno pareti cellulari quindi, in soluzioni ipotoniche, le cellule animali si gonfiano ed esplodono. Se troppa acqua entra nella cellula animale, questa può scoppiare - questo si chiama lisi. Non possono diventare turgidi perché non c'è parete cellulare per impedire alla cellula di scoppiare. Quando la cellula è in pericolo di scoppiare, gli organelli chiamati vacuoli contrattili pompano l'acqua fuori dalla cellula per evitare che ciò accada.
- Nelle soluzioni ipertoniche, l'acqua si diffonde fuori dalla cellula a causa dell'osmosi e la cellula si restringe. Se troppa acqua lascia la cellula animale, può ridursi - questo si chiama crenazione. Pertanto, la cellula animale deve sempre essere circondata da una soluzione isotonica. Nel corpo umano, i reni forniscono il meccanismo di regolazione necessario per il plasma sanguigno. La concentrazione di acqua e sale rimossa dal sangue dai reni è controllata da una parte del cervello chiamata ipotalamo. Il processo di regolazione della concentrazione di acqua e sali minerali nel sangue è chiamato osmoregolazione.
- Gli animali che vivono sulla terraferma devono conservare l'acqua, così come gli animali che vivono in acqua di mare salata. Gli animali che vivono in acqua dolce hanno il problema opposto; devono liberarsi dell'acqua in eccesso alla stessa velocità con cui entra nei loro corpi per osmosi.


