Цели на учење
Во оваа лекција, учениците ќе
- Опишете осмоза и осмотски притисок
- Опишете растворувач и сол
- Опишете решение и различни видови на решение
- Разберете го ефектот на осмоза во клетките на растението
- Разберете го ефектот на осмоза кај клетките на животните
Што е осмоза?
Осмозата е движење на вода од висока концентрација до ниска концентрација преку полупропустлива мембрана. Осмозата се однесува само на движење на молекули на вода. Тоа е посебен вид дифузија.
Тоа е пасивен транспорт што значи дека не бара енергија да се применува.
Разреден раствор содржи висока концентрација на молекули на вода, додека концентриран раствор содржи мала концентрација на молекули на вода.
Различните концентрации на соли од двете страни на мембраната предизвикуваат осмотски притисок. Кога се случува осмоза, водата се движи од страната на мембраната со помала количина на осмотски притисок на страната на мембраната со поголема количина осмотски притисок.
Кога концентрацијата на вода е иста од двете страни на мембраната, движењето на молекуларната вода ќе биде исто и во двете насоки. Нема да има нето движење на молекулите на водата.
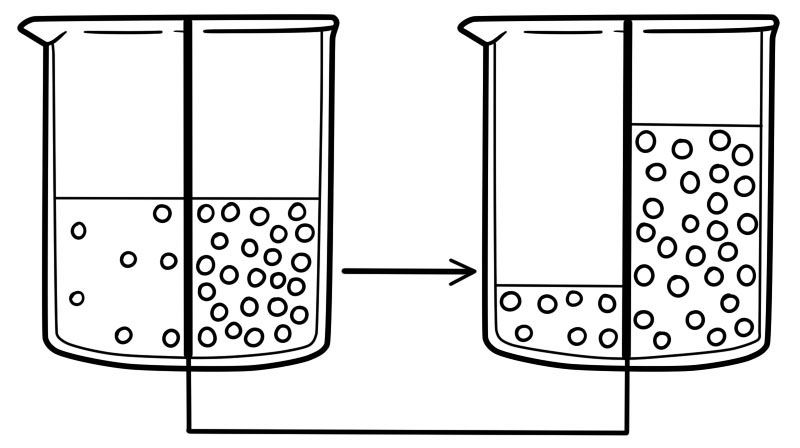
Осмоза низ живите клетки
Клетките содржат разредени раствори на јони, шеќери и аминокиселини.
Клеточната мембрана е делумно пропустлива. Водата ќе се пресели во и надвор од клетките со осмоза.
Важен пример за осмоза е движењето на течни (растворувач) молекули низ клеточна мембрана во клетка со поголема концентрација на сол.
Што е осмотски притисок?
Осмотскиот притисок е притисок што предизвикува дифузија на вода преку полупропустливи мембрани. Се зголемува како резултат на зголемување на концентрацијата на соли во растворот.
Што се растворувачи и растворувачи?
Осмозата се занимава со хемиски раствори. Решенијата имаат два дела - растворувач и сол.
Кога растворувачот се раствора во растворувач, крајниот производ се нарекува раствор. Солената вода е пример за решение; солта е солта, а водата е растворувач.
Кои се различните видови решенија?
Постојат три вида решенија за осмоза - изотоничен раствор, хипотоничен раствор и раствор на хипертоника. Различни видови на решенија имаат различни влијанија врз клетките како резултат на осмоза.
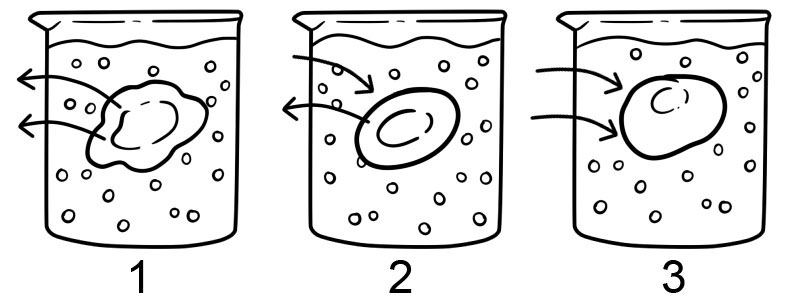
1. Хипертоничен - Хипертоничен раствор е спротивно на хипотоничен раствор; има повеќе солта надвор од ќелијата отколку во неа. Во овој вид на раствор, водата се движи надвор од ќелијата и предизвикува намалување на клетката.
2. Изотоничен - изотоничен раствор има иста концентрација на соли како во и надвор од клетката. Под овие услови, не постои нето движење на растворувач; во овој случај, количината на вода што влегува и излегува од мембраната на клетката е еднаква.
3. Хипотоничен - Во хипотоничен раствор, има поголема концентрација на соли во внатрешноста на ќелијата отколку надвор од клетката. Во хипотоничен раствор, водата се движи во ќелијата и може да предизвика клетката да отече; клетки кои немаат клеточен wallид, како што се животински клетки, би можеле да експлодираат во овој вид раствор.
Ефекти на осмоза во клетките на растението
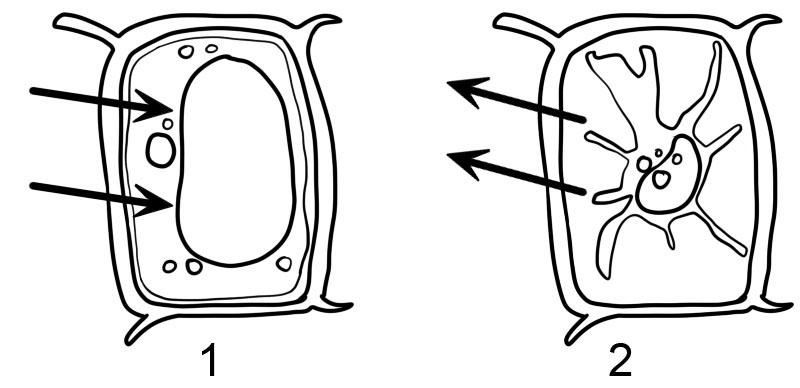
- Хипотоничен
- Хипертоничен
- Растителните клетки се затворени со цврст клеточен ид. Кога растителната ќелија се става во хипотоничен раствор, зафаќа вода со осмоза и почнува да отекува, но клеточниот ид спречува да пукне. За растителната клетка се вели дека станала „мачна“, т.е. отечена и тврда. Притисокот во внатрешноста на ќелијата се крева сè додека овој внатрешен притисок не е еднаков на притисокот надвор. Овој течен или хидростатички притисок се нарекува „притисок на тургор“ и го спречува понатамошниот нето-внес на вода.
- Нијатоста е многу важна за растенијата, бидејќи помага при одржување на цврстина и стабилност на растителното ткиво, и бидејќи секоја клетка врши притисок на тургор врз соседот, таа создава затегнатост на ткивото на растенијата што им овозможува на зелените делови на растението да „застанат“ на сончева светлина.
- Кога растителната ќелија се става во хипертоничен раствор, водата од внатре во цитоплазмата на клетката се шири и се вели дека растителната клетка станала „флакцидна“. Ако растителната клетка тогаш се набудува под микроскоп, ќе се забележи дека цитоплазмата се намали и се повлече од cellидот на клетката. Овој феномен се нарекува плазмолиза. Процесот се менува веднаш штом клетките се префрлаат во хипотоничен раствор (деплазмолиза).
- Кога растителната ќелија се става во изотоничен раствор, се вели дека се појавува феномен наречен „почетна плазмолиза“. „Почетник“ значи „ќе биде“. Иако ќелијата не е плазмозолирана, таа не е ниту мачна. Кога тоа се случи, зелените делови на растението се спуштаат и не се во состојба да ги држат лисјата нагоре под сончева светлина.
Ефекти на осмоза кај клетките на животните
- Cellsивотинските клетки немаат клеточни wallsидови, така, во хипотонични раствори, животинските клетки отекуваат и експлодираат. Ако премногу вода влезе во животинската ќелија може да пукне - ова се нарекува лиза. Тие не можат да станат заматени затоа што нема мобилен wallид за да спречи пукање на ќелијата. Кога ќелијата е во опасност од пукање, органелите наречени контрактилни вакуоли ќе испумпуваат вода од ќелијата за да спречат тоа да се случи.
- Во хипертонични раствори, водата се шири надвор од ќелијата поради осмоза и ќелијата се намалува. Ако премногу вода ја остава животинската клетка, може да се намали - ова се нарекува гајба. Така, животинската клетка секогаш мора да биде опкружена со изотоничен раствор. Во човечкото тело, бубрезите го обезбедуваат потребниот регулаторен механизам за крвната плазма. Концентрацијата на вода и сол отстранета од крвта од бубрезите ја контролира дел од мозокот наречен хипоталамус. Процесот на регулирање на концентрацијата на вода и минерални соли во крвта се нарекува осморгулација.
- Animивотните што живеат на суво земјиште мораат да штедат вода, како и животните што живеат во солена морска вода. Alsивотните што живеат во слатка вода имаат спротивен проблем; тие мора да се ослободат од вишокот вода толку брзо колку што влегува во нивните тела со осмоза.


