objetivos de aprendizado
Nesta aula, os alunos irão
- Descreva a osmose e a pressão osmótica
- Descrever solvente e soluto
- Descrever a solução e os diferentes tipos de solução
- Entenda o efeito da osmose nas células vegetais
- Entenda o efeito da osmose nas células animais
O que é osmose?
A osmose é o movimento da água de uma alta concentração para uma baixa concentração através de uma membrana semipermeável. A osmose refere-se apenas ao movimento das moléculas de água. É um tipo especial de difusão.
É um transporte passivo, o que significa que não requer energia para ser aplicada.
Uma solução diluída contém uma alta concentração de moléculas de água, enquanto uma solução concentrada contém uma baixa concentração de moléculas de água.
As diferentes concentrações de solutos nos dois lados da membrana causam pressão osmótica. Quando a osmose acontece, a água se move do lado da membrana com menor pressão osmótica para o lado da membrana com maior pressão osmótica.
Quando a concentração de água é a mesma em ambos os lados da membrana, o movimento molecular da água será o mesmo em ambas as direções. Não haverá movimento líquido de moléculas de água.
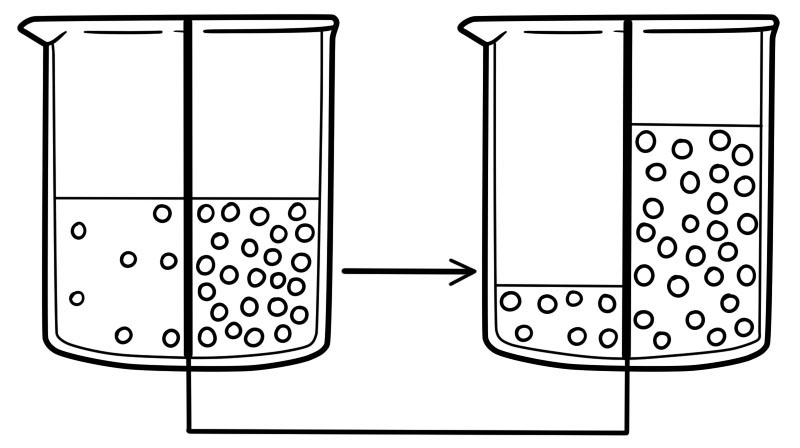
Osmose entre células vivas
As células contêm soluções diluídas de íons, açúcares e aminoácidos.
A membrana celular é parcialmente permeável. A água entrará e sairá das células por osmose.
Um exemplo importante de osmose é o movimento de moléculas líquidas (solventes) através de uma membrana celular para uma célula com maior concentração de soluto.
O que é pressão osmótica?
A pressão osmótica é a pressão que causa a difusão da água através de membranas semipermeáveis. Ela aumenta devido a um aumento na concentração de solutos na solução.
O que são solventes e solutos?
Osmose lida com soluções químicas. As soluções têm duas partes – um solvente e um soluto.
Quando um soluto se dissolve em um solvente, o produto final é chamado de solução. A água salgada é um exemplo de solução; sal é o soluto e a água é o solvente.
Quais são os diferentes tipos de soluções?
Existem três tipos de soluções de osmose - a solução isotônica, solução hipotônica e solução hipertônica. Diferentes tipos de soluções têm diferentes impactos nas células devido à osmose.
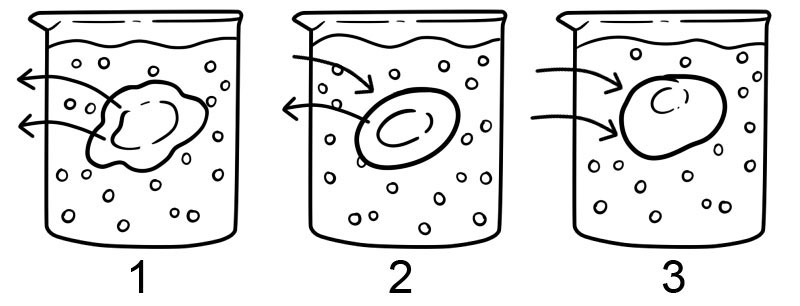
1. Hipertônica – Uma solução hipertônica é o oposto de uma solução hipotônica; há mais soluto fora da célula do que dentro dela. Nesse tipo de solução, a água se move para fora da célula e faz com que a célula murche.
2. Isotônico – Uma solução isotônica tem a mesma concentração de solutos dentro e fora da célula. Nessas condições, não há movimento líquido de solvente; neste caso, a quantidade de água que entra e sai da membrana da célula é igual.
3. Hipotônica – Em uma solução hipotônica, há uma maior concentração de solutos dentro da célula do que fora dela. Em uma solução hipotônica, a água se move para dentro da célula e pode fazer com que ela inche; células que não possuem parede celular, como células animais, podem explodir nesse tipo de solução.
Efeitos da osmose em células vegetais
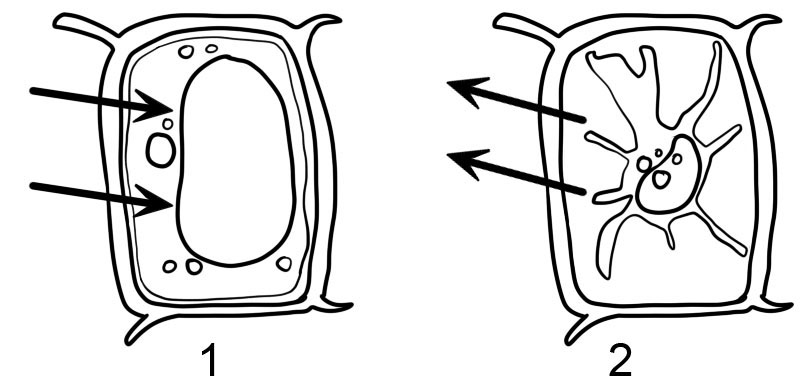
- Hipotônico
- Hipertônico
- As células vegetais são envolvidas por uma parede celular rígida. Quando a célula vegetal é colocada em uma solução hipotônica, ela absorve água por osmose e começa a inchar, mas a parede celular a impede de estourar. Diz-se que a célula da planta tornou-se 'túrgida', isto é, inchada e dura. A pressão dentro da célula aumenta até que essa pressão interna seja igual à pressão externa. Esta pressão líquida ou hidrostática é chamada de 'pressão de turgescência' e impede a entrada líquida adicional de água.
- A turgescência é muito importante para as plantas, pois ajuda na manutenção da rigidez e estabilidade do tecido vegetal e, à medida que cada célula exerce uma pressão de turgescência em seu vizinho, cria tensão no tecido vegetal que permite que as partes verdes da planta 'se levantem' para a luz do sol.
- Quando uma célula vegetal é colocada em uma solução hipertônica, a água de dentro do citoplasma da célula se difunde e diz-se que a célula vegetal se tornou “flácida”. Se a célula vegetal for observada ao microscópio, notará que o citoplasma encolheu e se afastou da parede celular. Esse fenômeno é chamado de plasmólise. O processo é revertido assim que as células são transferidas para uma solução hipotônica (desplasmólise).
- Quando uma célula vegetal é colocada em uma solução isotônica, diz-se que ocorre um fenômeno chamado “plasmólise incipiente”. 'Incipiente' significa 'prestes a ser'. Embora a célula não seja plasmoslisada, também não é túrgida. Quando isso acontece, as partes verdes da planta caem e são incapazes de segurar as folhas à luz do sol.
Efeitos da osmose em células animais
- As células animais não têm paredes celulares, então, em soluções hipotônicas, as células animais incham e explodem. Se muita água entrar na célula animal, ela pode explodir – isso é chamado de lise. Eles não podem ficar túrgidos porque não há parede celular para evitar que a célula estoure. Quando a célula corre o risco de estourar, organelas chamadas vacúolos contráteis bombeiam água para fora da célula para evitar que isso aconteça.
- Em soluções hipertônicas, a água se difunde para fora da célula devido à osmose e a célula encolhe. Se muita água sair da célula animal, ela pode encolher – isso é chamado de crenação. Assim, a célula animal sempre tem que ser cercada por uma solução isotônica. No corpo humano, os rins fornecem o mecanismo regulador necessário para o plasma sanguíneo. A concentração de água e sal removida do sangue pelos rins é controlada por uma parte do cérebro chamada hipotálamo. O processo de regulação da concentração de água e sais minerais no sangue é chamado de osmorregulação.
- Os animais que vivem em terra firme devem conservar água, assim como os animais que vivem em água salgada do mar. Os animais que vivem em água doce têm o problema oposto; eles devem se livrar do excesso de água tão rápido quanto ela entra em seus corpos por osmose.


