Mga Layunin sa pag-aaral
Sa araling ito, gagawin ng mga mag-aaral
- Ilarawan ang osmosis at osmotic pressure
- Ilarawan ang solvent at solute
- Ilarawan ang solusyon at iba't ibang uri ng solusyon
- Unawain ang epekto ng osmosis sa mga selula ng halaman
- Unawain ang epekto ng osmosis sa mga selula ng hayop
Ano ang osmosis?
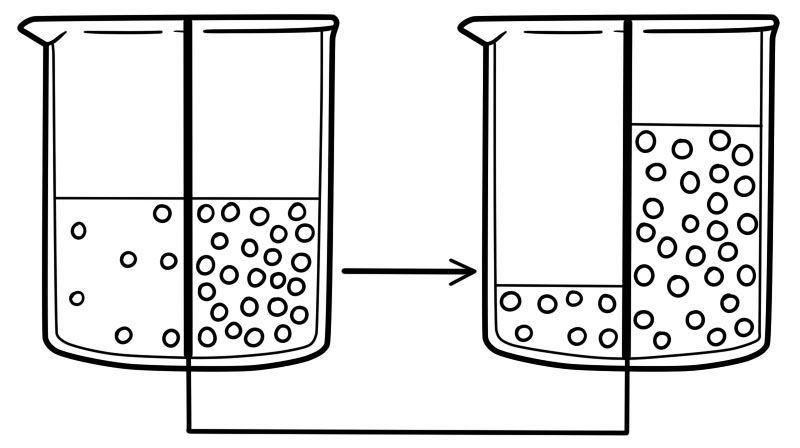
Ang Osmosis ay ang paggalaw ng tubig mula sa mataas na konsentrasyon hanggang sa mababang konsentrasyon sa pamamagitan ng semi-permeable membrane. Ang Osmosis ay tumutukoy sa paggalaw ng mga molekula ng tubig lamang. Ito ay isang espesyal na uri ng pagsasabog.
Ito ay passive transport na nangangahulugang hindi ito nangangailangan ng enerhiya upang mailapat.
Ang isang dilute na solusyon ay naglalaman ng mataas na konsentrasyon ng mga molekula ng tubig, habang ang isang puro solusyon ay naglalaman ng isang mababang konsentrasyon ng mga molekula ng tubig.
Ang iba't ibang konsentrasyon ng mga solute sa dalawang panig ng lamad ay nagdudulot ng osmotic pressure. Kapag nangyari ang osmosis, ang tubig ay gumagalaw mula sa gilid ng lamad na may mas mababang halaga ng osmotic pressure patungo sa gilid ng lamad na may mas mataas na halaga ng osmotic pressure.
Kapag ang konsentrasyon ng tubig ay pareho sa magkabilang panig ng lamad, ang paggalaw ng molekular ng tubig ay magiging pareho sa parehong direksyon. Hindi magkakaroon ng netong paggalaw ng mga molekula ng tubig.
Osmosis sa mga buhay na selula
Ang mga cell ay naglalaman ng mga dilute na solusyon ng mga ion, asukal, at amino acid.
Ang lamad ng cell ay bahagyang natatagusan. Ang tubig ay lilipat sa loob at labas ng mga selula sa pamamagitan ng osmosis.
Ang isang mahalagang halimbawa ng osmosis ay ang paggalaw ng mga likido (solvent) na molekula sa isang cell lamad sa isang cell na may mas mataas na konsentrasyon ng solute.
Ano ang osmotic pressure?
Ang osmotic pressure ay ang presyon na nagiging sanhi ng pagsasabog ng tubig sa pamamagitan ng mga semi-permeable na lamad. Tumataas ito dahil sa pagtaas ng konsentrasyon ng mga solute sa solusyon.
Ano ang mga solvents at solutes?
Ang Osmosis ay tumatalakay sa mga solusyong kemikal. Ang mga solusyon ay may dalawang bahagi - isang solvent, at isang solute.
Kapag ang isang solute ay natunaw sa isang solvent, ang huling produkto ay tinatawag na isang solusyon. Ang tubig-alat ay isang halimbawa ng solusyon; ang asin ang solute, at ang tubig ang solvent.
Ano ang iba't ibang uri ng solusyon?
May tatlong uri ng mga solusyon sa osmosis – ang isotonic solution, hypotonic solution, at hypertonic solution. Ang iba't ibang uri ng solusyon ay may iba't ibang epekto sa mga cell dahil sa osmosis.
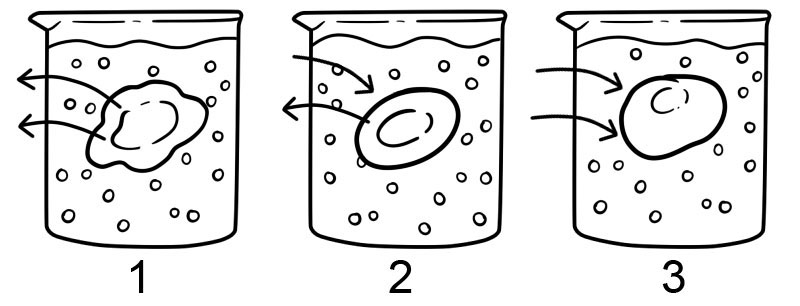
1. Hypertonic - Ang hypertonic solution ay ang kabaligtaran ng hypotonic solution; may mas maraming solute sa labas ng cell kaysa sa loob nito. Sa ganitong uri ng solusyon, ang tubig ay gumagalaw palabas ng cell at nagiging sanhi ng pagkatuyo ng cell.
2. Isotonic – Ang isotonic solution ay may parehong konsentrasyon ng mga solute sa loob at labas ng cell. Sa ilalim ng mga kundisyong ito, walang netong paggalaw ng solvent; sa kasong ito, ang dami ng tubig na pumapasok at lumalabas sa lamad ng cell ay pantay.
3. Hypotonic – Sa isang hipotonic solution, mayroong mas mataas na konsentrasyon ng mga solute sa loob ng cell kaysa sa labas ng cell. Sa isang hypotonic solution, ang tubig ay gumagalaw sa cell at maaaring maging sanhi ng paglaki ng cell; Ang mga cell na walang cell wall, gaya ng mga selula ng hayop ay maaaring sumabog sa ganitong uri ng solusyon.
Mga epekto ng osmosis sa mga selula ng halaman
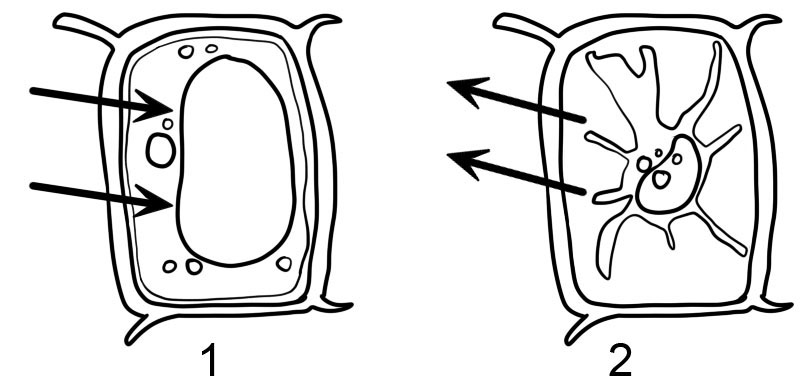
- Hypotonic
- Hypertonic
- Ang mga selula ng halaman ay napapalibutan ng isang matibay na pader ng selula. Kapag ang plant cell ay inilagay sa isang hypotonic solution, ito ay kumukuha ng tubig sa pamamagitan ng osmosis at nagsisimulang bumukol, ngunit pinipigilan ito ng cell wall na pumutok. Ang selula ng halaman ay sinasabing naging 'turgid' ibig sabihin ay namamaga at matigas. Ang presyon sa loob ng cell ay tumataas hanggang ang panloob na presyon ay katumbas ng presyon sa labas. Ang likido o hydrostatic pressure na ito ay tinatawag na 'turgor pressure' at pinipigilan nito ang karagdagang paggamit ng tubig.
- Napakahalaga ng turgidity sa mga halaman dahil nakakatulong ito sa pagpapanatili ng katigasan at katatagan ng tissue ng halaman, at habang ang bawat cell ay nagdudulot ng turgor pressure sa kapitbahay nito, lumilikha ito ng tensyon sa tissue ng halaman na nagpapahintulot sa mga berdeng bahagi ng halaman na 'tumayo' sa sikat ng araw.
- Kapag ang isang plant cell ay inilagay sa isang hypertonic solution, ang tubig mula sa loob ng cytoplasm ng cell ay diffuse out at ang plant cell ay sinasabing naging 'flaccid'. Kung ang selula ng halaman ay sinusunod sa ilalim ng mikroskopyo, mapapansin na ang cytoplasm ay lumiit at humiwalay sa dingding ng selula. Ang kababalaghang ito ay tinatawag na plasmolysis. Ang proseso ay nababaligtad sa sandaling ang mga selula ay inilipat sa isang hipotonik na solusyon (deplasmolysis).
- Kapag ang isang plant cell ay inilagay sa isang isotonic solution, isang phenomenon na tinatawag na "incipient plasmolysis' ay sinasabing magaganap. Ang ibig sabihin ng 'nagsisimula' ay 'malapit nang maging'. Kahit na ang cell ay hindi plasmoslysed, hindi rin ito turgid. Kapag nangyari ito, ang mga berdeng bahagi ng halaman ay nalalagas at hindi kayang hawakan ang mga dahon sa sikat ng araw.
Mga epekto ng osmosis sa mga selula ng hayop
- Ang mga selula ng hayop ay walang mga pader ng selula kaya, sa mga hipotonik na solusyon, ang mga selula ng hayop ay namamaga at sumasabog. Kung masyadong maraming tubig ang pumapasok sa selula ng hayop maaari itong sumabog - ito ay tinatawag na lysis. Hindi sila maaaring maging turgid dahil walang cell wall na pumipigil sa pagputok ng cell. Kapag ang cell ay nasa panganib ng pagsabog, ang mga organel na tinatawag na contractile vacuoles ay magbobomba ng tubig palabas ng cell upang maiwasang mangyari ito.
- Sa mga hypertonic solution, ang tubig ay kumakalat palabas ng cell dahil sa osmosis at lumiliit ang cell. Kung masyadong maraming tubig ang umalis sa selula ng hayop, maaari itong lumiit - ito ay tinatawag na crenation. Kaya, ang selula ng hayop ay dapat laging napapalibutan ng isotonic solution. Sa katawan ng tao, ang mga bato ay nagbibigay ng kinakailangang mekanismo ng regulasyon para sa plasma ng dugo. Ang konsentrasyon ng tubig at asin na inalis sa dugo ng mga bato ay kinokontrol ng isang bahagi ng utak na tinatawag na hypothalamus. Ang proseso ng pag-regulate ng konsentrasyon ng tubig at mga mineral na asing-gamot sa dugo ay tinatawag na osmoregulation.
- Ang mga hayop na nakatira sa tuyong lupa ay dapat magtipid ng tubig, tulad ng mga hayop na nakatira sa maalat na tubig-dagat. Ang mga hayop na nakatira sa tubig-tabang ay may kabaligtaran na problema; dapat nilang alisin ang labis na tubig nang kasing bilis ng pagpasok nito sa kanilang mga katawan sa pamamagitan ng osmosis.


