শিক্ষার উদ্দেশ্য
এই পাঠে আমরা শিখব
- এনজাইম কি?
- এনজাইমের প্রধান বৈশিষ্ট্য
- কিভাবে এনজাইম কাজ করে?
- লক এবং কী অনুমান
- প্ররোচিত-ফিট অনুমান
- মূল কারণগুলি যা এনজাইম কার্যকলাপকে প্রভাবিত করে
- ছয় রকমের এনজাইম
এনজাইম কি?
এনজাইম হল জৈবিক অনুঘটক যা প্রক্রিয়ায় নিজেদের পরিবর্তন না করে রাসায়নিক বিক্রিয়াগুলিকে গতি দেয়। একটি জীবন্ত ব্যবস্থা এনজাইমের মাধ্যমে তার কার্যকলাপ নিয়ন্ত্রণ করে।
এনজাইমের কিছু উদাহরণ হল
- ল্যাকটেজ - এটি ল্যাকটোজকে গ্লুকোজ এবং গ্যালাকটোসে বিভক্ত করে
- ক্যাটালেস - এটি হাইড্রোজেন পারক্সাইডকে পানি এবং অক্সিজেনে ভেঙ্গে দেয়
- গ্লাইকোজেন সিন্থেস - এটি গ্লুকোজ অণুর মধ্যে গ্লাইকোসিডিক বন্ধন গঠনের অনুঘটক
- ATPase - এটি ATP কে ADP তে ভেঙ্গে শক্তি উৎপাদন করে
এনজাইমের প্রধান বৈশিষ্ট্য কি?
- একটি এনজাইমের মৌলিক কাজ হল একটি বিক্রিয়া হার বৃদ্ধি করা।
- এনজাইমগুলি সুনির্দিষ্ট অর্থাৎ তাদের একটি নির্দিষ্ট আকৃতি আছে, তাই শুধুমাত্র একটি নির্দিষ্ট স্তর তার সক্রিয় সাইটে ফিট করবে
- এনজাইমগুলি কম কার্যকলাপের অবস্থা থেকে উচ্চ ক্রিয়াকলাপে এবং তদ্বিপরীতভাবে নিয়ন্ত্রিত হয়
কিভাবে এনজাইম কাজ করে?
একটি কোষের বেশিরভাগ প্রতিক্রিয়ার জন্য খুব উচ্চ তাপমাত্রার প্রয়োজন হয়, যা কোষকে ধ্বংস করে। এনজাইমগুলি বিক্রিয়াটির সক্রিয়করণ শক্তি কমিয়ে কাজ করে। একটি অণুর মধ্যে বন্ধনগুলির উপর চাপ প্রয়োগ করে, অথবা অণুগুলিকে একসাথে ধরে রাখার মাধ্যমে একটি প্রতিক্রিয়া সক্রিয়করণ শক্তি হ্রাস পায়। এটি একটি প্রতিক্রিয়ার সম্ভাবনা বাড়ায় এবং এটি শুরু করার জন্য প্রয়োজনীয় শক্তি হ্রাস করে।
যে অণু দিয়ে এনজাইম বাঁধে তাকে সাবস্ট্রেট বলা হয়। স্তরটি সক্রিয় সাইট হিসাবে উল্লেখিত এনজাইমের একটি ছোট অংশে আবদ্ধ। বিক্রিয়া শেষে উৎপন্ন অণুকে 'পণ্য' বলে। একবার প্রতিক্রিয়া সম্পূর্ণ হলে, এনজাইম পণ্যটি ছেড়ে দেয় এবং অন্য একটি স্তরের সাথে আবদ্ধ হওয়ার জন্য প্রস্তুত হয়।
এনজাইম ক্রিয়া ব্যাখ্যা করার জন্য দুটি তত্ত্ব রয়েছে
লক এবং কী থিওরি
এটি প্রথম এমিল ফিশার 1894 সালে পোস্ট করেছিলেন। লক এবং কী হাইপোথিসিস হল কিভাবে একটি এনজাইম অনুঘটক সাবস্ট্রেট প্রতিক্রিয়া। এটি বলে যে এনজাইমগুলির সক্রিয় সাইটগুলির আকারটি স্তরের আকারের ঠিক পরিপূরক। যখন একটি সাবস্ট্রেট অণু একটি এনজাইমের সাথে ধাক্কা খায় যার সক্রিয় সাইট আকৃতি পরিপূরক, স্তরটি সক্রিয় সাইটে ফিট হবে এবং একটি এনজাইম-সাবস্ট্রেট কমপ্লেক্স তৈরি হবে। এনজাইম প্রতিক্রিয়া অনুঘটক করবে, এবং পণ্যগুলি, এনজাইমের সাথে একত্রে একটি এনজাইম-পণ্য কমপ্লেক্স গঠন করবে। এই মডেল অনুসারে, একটি এনজাইমের পক্ষে একটি বিপরীত প্রতিক্রিয়া অনুঘটক করা সম্ভব।
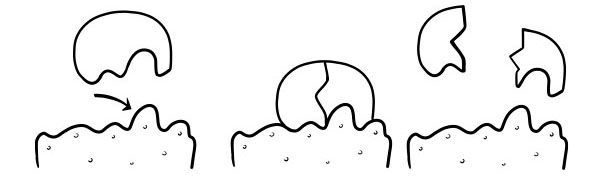
প্ররোচিত-ফিট হাইপোথিসিস
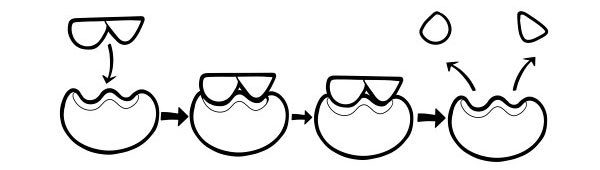
এনজাইমগুলি যেভাবে কাজ করে তা বর্ণনা করার জন্য এটি একটি অতি সাম্প্রতিক এবং ব্যাপকভাবে গৃহীত মডেল। এটি বলে যে সক্রিয় সাইটগুলির আকৃতি ঠিক পরিপূরক নয় কিন্তু একটি নির্দিষ্ট স্তরের উপস্থিতিতে আকৃতি পরিবর্তন করে পরিপূরক হয়ে ওঠে।
যখন একটি সাবস্ট্রেট অণু একটি এনজাইমের সাথে ধাক্কা খায়, যদি এর গঠন বিশেষভাবে সঠিক হয়, এনজাইমের সক্রিয় সাইটের আকৃতি পরিবর্তন হবে যাতে সাবস্ট্রেটটি তার সাথে খাপ খায় এবং একটি এনজাইম-সাবস্ট্রেট কমপ্লেক্স গঠন করতে পারে। প্রতিক্রিয়া তারপর অনুঘটক এবং একটি এনজাইম-পণ্য জটিল ফর্ম।
যে উপাদানগুলি এনজাইম কার্যকলাপকে প্রভাবিত করে
এনজাইম এবং সাবস্ট্রেটের পরিবেশ প্রতিক্রিয়ার গতিকে প্রভাবিত করতে পারে। কিছু কিছু ক্ষেত্রে, পরিবেশ এনজাইমকে কাজ বন্ধ করতে বা এমনকি উন্মোচন করতে পারে। যখন কোনো এনজাইম কাজ করা বন্ধ করে দেয়, তখন আমরা একে "বিকৃত" বলি।
এখানে কিছু বিষয় আছে যা এনজাইম কার্যকলাপকে প্রভাবিত করতে পারে:
- তাপমাত্রা - তাপমাত্রা প্রতিক্রিয়া হারকে প্রভাবিত করতে পারে। তাপমাত্রা যত বেশি হবে, প্রতিক্রিয়া তত দ্রুত হবে। যাইহোক, একটি সহনীয় সীমার বাইরে তাপমাত্রা বৃদ্ধি বা হ্রাস সক্রিয় সাইটের রাসায়নিক বন্ধনগুলিকে প্রভাবিত করতে পারে, যা তাদের স্তরগুলি আবদ্ধ করার জন্য কম উপযুক্ত করে তোলে। খুব উচ্চ তাপমাত্রা একটি এনজাইমকে বিকৃত করতে পারে, এর আকৃতি এবং ক্রিয়াকলাপ হারায়।
- pH - pH এনজাইম ফাংশনকেও প্রভাবিত করতে পারে। সক্রিয় সাইট অ্যামিনো অ্যাসিডের অবশিষ্টাংশে প্রায়ই অ্যাসিডিক বা মৌলিক বৈশিষ্ট্য থাকে যা ক্যাটালাইসিসের জন্য গুরুত্বপূর্ণ। পিএইচ -তে পরিবর্তন এই অবশিষ্টাংশগুলিকে প্রভাবিত করতে পারে এবং সাবস্ট্রেটগুলিকে আবদ্ধ করা কঠিন করে তোলে। এনজাইমগুলি একটি নির্দিষ্ট পিএইচ রেঞ্জের মধ্যে সবচেয়ে ভাল কাজ করে এবং তাপমাত্রার মতো, চরম পিএইচ মান (অম্লীয় বা মৌলিক) এনজাইমগুলিকে বিকৃত করতে পারে।
- এনজাইম এবং সাবস্ট্রেটের ঘনত্ব - একটি বিন্দু পর্যন্ত সাবস্ট্রেট ঘনত্ব বৃদ্ধির সাথে প্রতিক্রিয়া হার বৃদ্ধি পায়, যার বাইরে স্তরের ঘনত্বের আরও বৃদ্ধি প্রতিক্রিয়া হারে উল্লেখযোগ্য পরিবর্তন আনতে পারে না। এটি ঘটে কারণ স্তরের একটি নির্দিষ্ট ঘনত্বের পরে, এনজাইমের সমস্ত সক্রিয় সাইটগুলি পূর্ণ হয়ে যায় এবং আর কোনও প্রতিক্রিয়া ঘটতে পারে না।
- ইনহিবিটারস - ইনহিবিটর হলো অণু যা বিশেষভাবে এনজাইমের কার্যকলাপ বন্ধ করার জন্য তৈরি করা হয়। তারা কেবল প্রতিক্রিয়াটি ধীর করে দিতে পারে বা এটি পুরোপুরি বন্ধ করতে পারে। কিছু ইনহিবিটর এনজাইমের সাথে বন্ধন করে যার ফলে এটি আকৃতি পরিবর্তন করে এবং সঠিকভাবে কাজ করে না। একটি ইনহিবিটারের বিপরীত হল একটি অ্যাক্টিভেটর যা প্রতিক্রিয়া দ্রুত করতে সাহায্য করতে পারে।
এনজাইমের ধরন
মানবদেহ ছয়টি প্রধান গ্রুপ বা এনজাইমের শ্রেণী নিয়ে গঠিত:
- অক্সিডোরডাক্টেসেস - এই এনজাইমগুলি জারণ এবং হ্রাস প্রতিক্রিয়াগুলির হার বাড়ায়। এই প্রতিক্রিয়াগুলিতে, যাকে রেডক্স বিক্রিয়াও বলা হয়, প্রতিক্রিয়াশীলদের মধ্যে একটি ইলেকট্রনের একটি জোড়া ছেড়ে দেয় যা অন্য প্রতিক্রিয়াশীল লাভ করে। ইলেকট্রন-জোড়া দাতা অক্সিডাইজড বলে এবং একটি হ্রাসকারী এজেন্ট হিসাবে কাজ করে, যখন ইলেকট্রন-জোড়া গ্রহীতা হ্রাস পায় তাকে বলা হয় অক্সিডাইজিং এজেন্ট। উদাহরণগুলির মধ্যে রয়েছে সাইটোক্রোম অক্সিডেস এবং ল্যাকটেট ডিহাইড্রোজেনেস।
- স্থানান্তর - এই এনজাইমগুলি পরমাণুর গোষ্ঠী যেমন মিথাইল (সিএইচ 3 ), অ্যাসিটাইল (সিএইচ 3 সিও) বা অ্যামিনো (এনএইচ 2 ) গোষ্ঠীর স্থানান্তরের সাথে এক অণু থেকে অন্য অণুতে গতি বাড়ায়। অ্যাসিটেট কিনেস এবং অ্যালানাইন ডিমিনেস হস্তান্তরগুলির উদাহরণ।
- হাইড্রোলাসেস - এই এনজাইমগুলি হাইড্রোলাইসিস প্রতিক্রিয়াগুলিকে ত্বরান্বিত করে। হাইড্রোলাইসিস বিক্রিয়া জল (H 2 O) ব্যবহার করে একটি অণুতে একটি বন্ধন বিভক্ত করে দুই কন্যা পণ্য তৈরি করে, সাধারণত জল থেকে -OH (হাইড্রোক্সিল গ্রুপ) জল থেকে একটি পণ্য এবং একক -H (হাইড্রোজেন পরমাণু) সংযুক্ত করে অন্যটি. ইতিমধ্যে, -H এবং -OH উপাদান দ্বারা স্থানচ্যুত পরমাণু থেকে একটি নতুন অণু গঠিত হয়। হজমকারী এনজাইম লিপেজ এবং সুক্রাস হাইড্রোলাস।
- লায়াস - এই এনজাইমগুলি একটি আণবিক গোষ্ঠীর সংযোজনের হারকে একটি দ্বৈত বন্ধনে বা নিকটবর্তী পরমাণু থেকে দুটি গোষ্ঠীকে অপসারণ করে একটি দ্বৈত বন্ধন তৈরি করে। এগুলি হাইড্রোলাসেসের মতো কাজ করে, তবে বাদ দেওয়া উপাদান জল বা পানির অংশ দ্বারা স্থানচ্যুত হয় না। এই শ্রেণীর এনজাইমের মধ্যে রয়েছে অক্সালেট ডিকারবক্সাইলেজ এবং আইসোসিট্রেট লাইজ।
- আইসোমেরেসেস - এই এনজাইমগুলি আইসোমারাইজেশন প্রতিক্রিয়াগুলিকে গতি দেয়। এগুলি হল এমন প্রতিক্রিয়া যেখানে বিক্রিয়কের সমস্ত মূল পরমাণুগুলি ধরে রাখা হয়, তবে বিক্রিয়কের আইসোমার গঠনের জন্য পুনর্বিন্যাস করা হয়। Isomers একই রাসায়নিক সূত্র সঙ্গে অণু, কিন্তু বিভিন্ন ব্যবস্থা। উদাহরণগুলির মধ্যে রয়েছে গ্লুকোজ-ফসফেট আইসোমারেজ এবং অ্যালানাইন রেসমেজ।
- লিগেস - সিনথেটেস নামেও পরিচিত, এই এনজাইম দুটি অণুর যোগদানের হার বাড়ায়। তারা সাধারণত এডিনোসিন ট্রাইফসফেট (এটিপি) এর ভাঙ্গন থেকে প্রাপ্ত শক্তির ব্যবহার করে এটি সম্পন্ন করে। লিগেসের উদাহরণগুলির মধ্যে রয়েছে অ্যাসিটাইল-সিওএ সিনথেটেজ এবং ডিএনএ লিগেজ।

