Mga Layunin sa pag-aaral
Sa araling ito, matututuhan natin
- Ano ang mga enzymes?
- Mga pangunahing katangian ng mga enzyme
- Paano gumagana ang mga enzyme?
- Lock at Key Hypothesis
- Induced-Fit Hypothesis
- Mga pangunahing salik na nakakaapekto sa aktibidad ng enzyme
- Anim na iba't ibang uri ng enzymes
ANO ANG ENZYMES?
Ang mga enzyme ay mga biological catalyst na nagpapabilis sa mga reaksiyong kemikal nang hindi sila nagbabago sa proseso. Kinokontrol ng isang buhay na sistema ang aktibidad nito sa pamamagitan ng mga enzyme.
Ang ilang mga halimbawa ng mga enzyme ay
- Lactase - Pinaghihiwa nito ang Lactose sa Glucose at Galactose
- Catalase – Binabagsak nito ang hydrogen peroxide sa tubig at oxygen
- Glycogen synthase - Pinapaandar nito ang pagbuo ng mga glycosidic bond sa pagitan ng mga molekula ng glucose
- ATPase – Binababagsak nito ang ATP sa ADP, na gumagawa ng enerhiya
ANO ANG MGA PANGUNAHING KATANGIAN NG ENZYMES?
- Ang pangunahing pag-andar ng isang enzyme ay upang mapataas ang rate ng isang reaksyon.
- Ang mga enzyme ay tiyak, ibig sabihin, mayroon silang isang tiyak na hugis, kaya isang tiyak na substrate lamang ang magkasya sa aktibong site nito
- Ang mga enzyme ay kinokontrol mula sa isang estado ng mababang aktibidad hanggang sa mataas na aktibidad at vice versa
PAANO GUMAGANA ANG MGA ENZYME?
Karamihan sa mga reaksyon sa isang cell ay nangangailangan ng napakataas na temperatura upang magpatuloy, na sisira sa cell. Ang mga enzyme ay gumagana sa pamamagitan ng pagpapababa ng activation energy ng isang reaksyon. Ang activation energy ng isang reaksyon ay nababawasan sa pamamagitan ng paglalagay ng stress sa mga bono sa loob ng isang molekula, o sa pamamagitan ng pagdikit ng mga molekula. Pinapataas nito ang posibilidad ng isang reaksyon at sa gayon ay nagpapababa ng enerhiya na kinakailangan upang simulan ito.
Ang molekula kung saan nakagapos ang enzyme ay tinutukoy bilang substrate. Ang substrate ay nagbubuklod sa isang maliit na seksyon ng enzyme na tinutukoy bilang aktibong site. Ang molekula na ginawa sa dulo ng reaksyon ay tinatawag na 'produkto'. Kapag nakumpleto na ang reaksyon, inilalabas ng enzyme ang produkto at handa nang magbigkis sa isa pang substrate.
Mayroong dalawang mga teorya upang ipaliwanag ang pagkilos ng enzyme
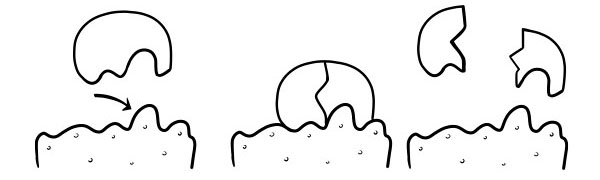
LOCK AND KEY THEORY
Ito ay unang ipinostula noong 1894 ni Emil Fischer. Ang Lock and Key Hypothesis ay isang modelo kung paano ang mga enzymes catalyst substrate reactions. Ito ay nagsasaad na ang hugis ng mga aktibong site ng mga enzyme ay eksaktong pantulong sa hugis ng substrate. Kapag ang isang molekula ng substrate ay bumangga sa isang enzyme na ang aktibong hugis ng site ay komplementaryo, ang substrate ay magkakasya sa aktibong site at isang enzyme-substrate complex ay mabubuo. Ang enzyme ay magpapagana sa reaksyon, at ang mga produkto, kasama ang enzyme ay bubuo ng enzyme-product complex. Ayon sa modelong ito, posible para sa isang enzyme na mag-catalyze ng reverse reaction.
INDUCED-FIT HYPOTHESIS
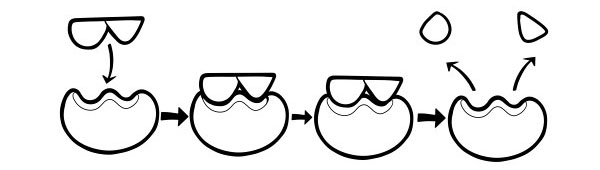
Ito ay isang mas bago at malawak na tinatanggap na modelo upang ilarawan ang paraan ng paggana ng mga enzyme. Ito ay nagsasaad na ang hugis ng mga aktibong site ay hindi eksaktong komplementaryo ngunit nagbabago ng hugis sa pagkakaroon ng isang tiyak na substrate upang maging komplementaryo.
Kapag ang isang molekula ng substrate ay bumangga sa isang enzyme, kung ang komposisyon nito ay partikular na tama, ang hugis ng aktibong site ng enzyme ay magbabago upang ang substrate ay magkasya sa nito at maaaring mabuo ang isang enzyme-substrate complex. Ang reaksyon ay pagkatapos ay catalyzed at isang enzyme-product complex form.
MGA SALIK NA NAKAKAAPEKTO SA AKTIBIDAD NG ENZYME
Ang kapaligiran ng enzyme at ang substrate ay maaaring makaapekto sa bilis ng reaksyon. Sa ilang mga kaso, ang kapaligiran ay maaaring maging sanhi ng enzyme na huminto sa paggana o kahit na malutas. Kapag huminto sa paggana ang isang enzyme, tinatawag natin itong "denatured".
Narito ang ilang salik na maaaring makaapekto sa aktibidad ng enzyme:
- Temperatura – Maaaring makaapekto ang temperatura sa rate ng reaksyon. Kung mas mataas ang temperatura, mas mabilis ang reaksyon na magaganap. Gayunpaman, ang alinman sa pagtaas o pagbaba ng temperatura sa labas ng isang matitiis na saklaw ay maaaring makaapekto sa mga bono ng kemikal sa aktibong site, na ginagawang hindi gaanong angkop ang mga ito upang magbigkis ng mga substrate. Ang napakataas na temperatura ay maaaring maging sanhi ng pag-denatur ng isang enzyme, na nawawala ang hugis at aktibidad nito.
- pH - Ang pH ay maaari ding makaapekto sa function ng enzyme. Ang mga residue ng amino acid sa aktibong site ay kadalasang may acidic o pangunahing mga katangian na mahalaga para sa catalysis. Ang mga pagbabago sa pH ay maaaring makaapekto sa mga residue na ito at maging mahirap para sa mga substrate na magbigkis. Pinakamahusay na gumagana ang mga enzyme sa loob ng isang partikular na hanay ng pH, at tulad ng temperatura, ang mga matinding halaga ng pH (acidic o basic) ay maaaring gumawa ng mga enzyme na denature.
- Ang konsentrasyon ng mga enzyme at substrate - Ang rate ng reaksyon ay tumataas sa pagtaas ng konsentrasyon ng substrate hanggang sa isang punto, kung saan ang anumang karagdagang pagtaas sa konsentrasyon ng substrate ay hindi gumagawa ng makabuluhang pagbabago sa rate ng reaksyon. Nangyayari ito dahil pagkatapos ng isang tiyak na konsentrasyon ng substrate, ang lahat ng mga aktibong site sa enzyme ay puno at walang karagdagang reaksyon ang maaaring mangyari.
- Inhibitor - Ang mga inhibitor ay mga molekula na espesyal na ginawa upang ihinto ang aktibidad ng mga enzyme. Maaari lamang nilang pabagalin ang reaksyon o ihinto ito nang buo. Ang ilang mga inhibitor ay nagbubuklod sa enzyme na nagiging sanhi ng pagbabago ng hugis nito at hindi gumagana ng tama. Ang kabaligtaran ng isang inhibitor ay isang activator na makakatulong upang mapabilis ang reaksyon.
MGA URI NG ENZYME
Ang katawan ng tao ay binubuo ng anim na pangunahing grupo o klase ng mga enzyme:
- Oxidoreductases - Ang mga enzyme na ito ay nagpapahusay sa rate ng oksihenasyon at pagbabawas ng mga reaksyon. Sa mga reaksyong ito, na tinatawag ding redox reactions, ang isa sa mga reactant ay nagbibigay ng isang pares ng mga electron na nakuha ng isa pang reactant. Ang electron-pair donor ay sinasabing oxidized at gumaganap bilang isang reducing agent, habang ang electron-pair na tatanggap ay nabawasan ay tinatawag na oxidizing agent. Kasama sa mga halimbawa ang cytochrome oxidase at lactate dehydrogenase.
- Transferases – Ang mga enzyme na ito ay bumibilis kasama ng paglilipat ng mga grupo ng mga atom, tulad ng methyl (CH 3 ), acetyl (CH 3 CO) o amino (NH 2 ) na mga grupo, mula sa isang molekula patungo sa isa pang molekula. Ang acetate kinase at alanine deaminase ay mga halimbawa ng transferases.
- Hydrolases - Ang mga enzyme na ito ay nagpapabilis ng mga reaksyon ng hydrolysis. Ang mga reaksyon ng hydrolysis ay gumagamit ng tubig (H 2 O) upang hatiin ang isang bono sa isang molekula upang lumikha ng dalawang anak na produkto, kadalasan sa pamamagitan ng paglalagay ng -OH (hydroxyl group) mula sa tubig sa isa sa mga produkto at isang solong -H (hydrogen atom) sa Yung isa. Samantala, ang isang bagong molekula ay nabuo mula sa mga atomo na inilipat ng mga sangkap -H at -OH. Ang mga digestive enzymes na lipase at sucrase ay hydrolases.
- Lyases - Pinapahusay ng mga enzyme na ito ang rate ng pagdaragdag ng isang molecular group sa isang double bond o ang pagtanggal ng dalawang grupo mula sa mga kalapit na atoms upang lumikha ng double bond. Ang mga ito ay kumikilos tulad ng mga hydrolase, maliban na ang inalis na bahagi ay hindi inilipat ng tubig o mga bahagi ng tubig. Kasama sa klase ng mga enzyme ang oxalate decarboxylase at isocitrate lyase.
- Isomerases - Ang mga enzyme na ito ay nagpapabilis ng mga reaksyon ng isomerization. Ito ay mga reaksyon kung saan ang lahat ng orihinal na mga atomo sa reactant ay pinanatili, ngunit muling inayos upang bumuo ng isang isomer ng reactant. Ang mga isomer ay mga molekula na may parehong pormula ng kemikal, ngunit magkaibang pagkakaayos. Kasama sa mga halimbawa ang glucose-phosphate isomerase at alanine racemase.
- Ligases - Tinatawag din na synthetases, pinapahusay ng mga enzyme na ito ang rate ng pagsali ng dalawang molekula. Karaniwang ginagawa nila ito sa pamamagitan ng paggamit ng enerhiya na nagmula sa pagkasira ng adenosine triphosphate (ATP). Kabilang sa mga halimbawa ng ligase ang acetyl-CoA synthetase at DNA ligase.

