سیکھنے کے مقاصد
اس سبق میں ، ہم سیکھیں گے
- خامروں کیا ہیں؟
- خامروں کی اہم خصوصیات
- خامروں سے کیسے کام ہوتا ہے؟
- لاک اور کلی مفروضے
- حوصلہ افزائی ہائپوٹیسس
- انزائم سرگرمی کو متاثر کرنے والے کلیدی عوامل
- خامروں کی چھ مختلف اقسام
خاکے کیا ہیں؟
انزائم حیاتیاتی کاتالک ہیں جو خود کو اس عمل میں ردوبدل کیے بغیر کیمیائی رد عمل کو تیز کرتے ہیں۔ ایک نظام زندگی انزائیمز کے ذریعے اپنی سرگرمی کو کنٹرول کرتا ہے۔
خامروں کی کچھ مثالیں یہ ہیں
- لییکٹیج - یہ لییکٹوز کو گلوکوز اور گیلیکٹوز میں توڑ دیتا ہے
- کاتالاس۔ یہ ہائیڈروجن پیرو آکسائیڈ کو پانی اور آکسیجن میں توڑ دیتا ہے
- گلیکوجن ترکیب - یہ گلوکوز انووں کے مابین گلیکوسیڈک بانڈز کی تشکیل کو تشکیل دیتا ہے۔
- اٹپیس - یہ توانائی پیدا کرنے والے اے ٹی پی کو اے ڈی پی میں توڑ دیتا ہے
انزائیمز کی اہم خصوصیات کیا ہیں؟
- ایک انزائم کا بنیادی کام رد عمل کی شرح میں اضافہ کرنا ہے۔
- انزائم مخصوص ہیں یعنی ان کی ایک مخصوص شکل ہوتی ہے ، لہذا اس کی فعال سائٹ پر صرف ایک مخصوص ذیلی سیٹ فٹ بیٹھتی ہے
- خامروں کو کم سرگرمی کی حالت سے لے کر اعلی سرگرمی تک منظم کیا جاتا ہے اور اس کے برعکس
کس طرح کام کرتے ہیں؟
کسی سیل میں زیادہ تر ردtions عمل کے ل بہت زیادہ درجہ حرارت کی ضرورت ہوتی ہے ، جو سیل کو ختم کردیتی ہے۔ انزائیم ایک رد عمل کی ایکٹیویشن انرجی کو کم کرکے کام کرتے ہیں۔ کسی انو کے اندر بانڈز پر دباؤ ڈال کر یا انووں کو قریب رکھتے ہوئے رد عمل کی ایکٹیویشن انرجی کو کم کیا جاتا ہے۔ اس سے کسی رد عمل کا امکان بڑھ جاتا ہے اور اس کے آغاز کے لئے درکار توانائی کم ہوجاتی ہے۔
انو انو جس کے ساتھ انزائم پابند ہوتا ہے اسے سبسٹریٹ کہا جاتا ہے۔ سبزٹریٹ انزیم کے ایک چھوٹے سے حصے سے جڑا ہوا ہے جسے فعال سائٹ کہا جاتا ہے۔ رد عمل کے اختتام پر پیدا ہونے والے انو کو 'پروڈکٹ' کہا جاتا ہے۔ ایک بار جب ردعمل مکمل ہوجاتا ہے تو ، انزائم مصنوع کو جاری کرتا ہے اور کسی دوسرے سبسٹریٹ کے ساتھ باندھنے کے لئے تیار ہوجاتا ہے۔
انزائم عمل کی وضاحت کرنے کے لئے دو نظریات ہیں
لاک اور کلیدی تھیوری
اسے پہلی بار 1894 میں ایمل فشر نے پوسٹ کیا تھا۔ لاک اور کلی مفروضہ اس بات کا ایک ماڈل ہے کہ کس طرح خامروں نے کتلسٹ سبسٹریٹ رد عمل ظاہر کیا۔ اس میں کہا گیا ہے کہ خامروں کے فعال مقامات کی شکل سبسٹریٹ کی شکل کے قطعی معاون ہے۔ جب سبسٹریٹ مالیکیول انزائم سے ٹکرا جاتا ہے جس کی فعال سائٹ کی شکل تکمیلی ہوتی ہے ، تو سبسٹریٹ فعال سائٹ میں فٹ ہوجاتا ہے اور ایک انزائم سبسٹریٹ کمپلیکس تشکیل پاتا ہے۔ انزیم رد عمل کو اتپریرک کردے گا ، اور مصنوعات انزیم کے ساتھ مل کر ایک انزائم پروڈکٹ کمپلیکس تشکیل دیں گے۔ اس ماڈل کے مطابق ، یہ ممکن ہے کہ کسی انزیم کا الٹا رد reactionی پیدا ہو۔
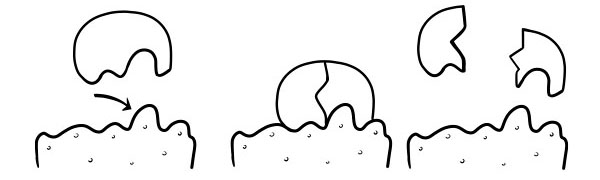
ہچکچائے ہوئے فٹ
خامروں کے کام کرنے کے طریقے کو بیان کرنے کے لئے یہ ایک حالیہ اور وسیع پیمانے پر قبول شدہ ماڈل ہے۔ اس میں کہا گیا ہے کہ فعال مقامات کی شکل قطعی طور پر تکمیلی نہیں ہوتی ہے بلکہ تکمیلی بننے کے ل a کسی مخصوص سبسٹریٹ کی موجودگی میں شکل کو تبدیل کرتی ہے۔
جب سبزٹریٹ مالیکیول ایک انزائم سے ٹکرا جاتا ہے ، اگر اس کی تشکیل خاص طور پر درست ہے تو ، انزائم کے فعال مقام کی شکل بدل جائے گی تاکہ سبسٹریٹ اس میں فٹ ہوجائے اور ایک انزائم سبسٹریٹ کمپلیکس تشکیل پائے۔ اس کے بعد رد عمل کیٹا لیز اور ایک انزائم پروڈکٹ پیچیدہ شکل ہے۔
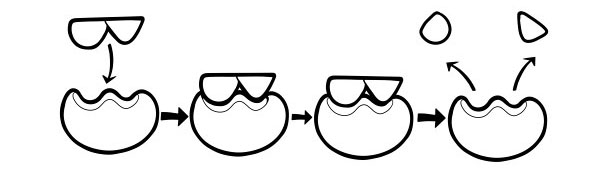
فیکٹرز جو ماحولیاتی سرگرمی کو متاثر کرتے ہیں
انزائم اور سبسٹریٹ کا ماحول رد عمل کی رفتار کو متاثر کرسکتا ہے۔ کچھ معاملات میں ، ماحول انزائیم کا کام کرنا بند کر دیتا ہے یا یہاں تک کہ نحوست کا باعث بن سکتا ہے۔ جب ایک انزائم کام کرنا چھوڑ دیتا ہے تو ، ہم اسے "ڈینچرڈ" کہتے ہیں۔
یہ کچھ عوامل ہیں جو انزائم سرگرمی کو متاثر کرسکتے ہیں۔
- درجہ حرارت - درجہ حرارت رد عمل کی شرح کو متاثر کرسکتا ہے۔ درجہ حرارت جتنا زیادہ ہوگا ، ردعمل اتنا ہی تیز ہوگا۔ تاہم ، یا تو کسی قابل برداشت حد سے باہر درجہ حرارت میں اضافہ یا کمی سے فعال سائٹ میں کیمیائی پابندیوں کو متاثر کیا جاسکتا ہے ، جس سے وہ پابند ذیلی علاقوں کو کم مناسب نہیں بناسکتے ہیں۔ بہت زیادہ درجہ حرارت کی وجہ سے ایک انزائم انکار ہوجاتا ہے ، جس کی شکل اور سرگرمی ختم ہوجاتی ہے۔
- پییچ - پییچ انزائیم فنکشن کو بھی متاثر کرسکتا ہے۔ ایکٹو سائٹ امینو ایسڈ کی اوشیشوں میں اکثر تیزابیت یا بنیادی خصوصیات ہوتی ہیں جو کٹلیسس کے ل important اہم ہیں۔ پییچ میں بدلاؤ ان اوشیشوں کو متاثر کرسکتا ہے اور سبسٹریٹس کو باندھنا مشکل بنا دیتا ہے۔ انزائمز ایک خاص پییچ کی حد میں بہترین کام کرتے ہیں ، اور درجہ حرارت کی طرح ، انتہائی پییچ اقدار (تیزابیت یا بنیادی) انزائیمز کی نشاندہی کرسکتے ہیں۔
- خامروں اور سبسٹریٹ کی حراستی - ایک نقطہ تک بڑھتے ہوئے سبسٹریٹ حراستی کے ساتھ رد عمل کی شرح بڑھ جاتی ہے ، اس سے آگے بھی سبسٹریٹ حراستی میں مزید اضافہ رد عمل کی شرح میں کوئی خاص تبدیلی نہیں پیدا کرتا ہے۔ ایسا ہوتا ہے کیونکہ سبسٹریٹ کی ایک خاص حراستی کے بعد ، خامروں میں موجود تمام فعال سائٹیں بھری ہوتی ہیں اور اس کے بعد کوئی اور رد reactionعمل نہیں ہوسکتا ہے۔
- رکاوٹیں پیدا کرنے والے ۔ انابائٹرز وہ انو ہوتے ہیں جو خامروں کی سرگرمی کو روکنے کے لئے خصوصی طور پر بنائے جاتے ہیں۔ وہ شاید ردعمل کو کم کریں یا اسے مکمل طور پر روکیں۔ کچھ روکنے والے انزائم کے ساتھ بانڈ کرتے ہیں جس کی وجہ سے اس کی شکل تبدیل ہوتی ہے اور صحیح کام نہیں ہوتا ہے۔ ایک روکنے والا کے برعکس ایک ایکٹیویٹر ہوتا ہے جو رد عمل کو تیز کرنے میں مدد کرسکتا ہے۔
عناصر کی اقسام
انسانی جسم چھ بڑے گروہوں یا خامروں کی کلاسوں پر مشتمل ہے۔
- آکسیڈور اغاز - یہ خامر آکسیکرن اور کمی رد عمل کی شرح کو بڑھاتے ہیں۔ ان رد عمل میں ، جسے ریڈوکس ری ایکشن بھی کہا جاتا ہے ، ایک ری ایکٹنٹ الیکٹران کا ایک جوڑا چھوڑ دیتا ہے جس سے دوسرا ری ایکٹنٹ حاصل ہوتا ہے۔ کہا جاتا ہے کہ الیکٹران جوڑی ڈونر کو آکسائڈائزڈ کیا جاتا ہے اور کم کرنے والے ایجنٹ کے طور پر کام کرتا ہے ، جبکہ الیکٹران جوڑی وصول کرنے والے کو کم کیا جاتا ہے جسے آکسائڈائزنگ ایجنٹ کہا جاتا ہے۔ مثالوں میں سائٹوکوم آکسیڈیز اور لییکٹٹیٹ ہائیڈروجنیز شامل ہیں۔
- تغیرات - یہ انزائیمز جوہری کے گروپس جیسے میتھیل (CH 3 ) ، ایسٹیل (CH CH 3 ) یا امینو (NH 2 ) گروپس کے ایک انو سے دوسرے انو میں منتقلی کے ساتھ تیز ہوجاتے ہیں۔ ایسیٹیٹ کنیز اور الانائن ڈیمینیز ٹرانسفرس کی مثال ہیں۔
- ہائڈروالس - یہ انزائم ہائیڈروالیسس رد عمل کو تیز کرتے ہیں۔ ہائیڈرولیسس رد عمل دو بیٹیوں کی مصنوعات تیار کرنے کے لئے انو میں بانڈ تقسیم کرنے کے لئے پانی (H 2 O) کا استعمال کرتے ہیں ، عام طور پر پانی سے ایک OH (ہائڈروکسل گروپ) کو کسی ایک مصنوعات سے جوڑ دیتے ہیں اور سنگل- H (ہائیڈروجن ایٹم) سے دیگر. اس دوران ، ایچ اور او او اجزاء کے ذریعہ بے گھر ہونے والے ایٹموں سے ایک نیا انو تشکیل پاتا ہے۔ ہاضم انزائمز لپیس اور سوکراس ہائیڈروولیس ہیں۔
- لیائسز - یہ انزائم ایک آناختی گروہ کے اضافے کی شرح کو ڈبل بانڈ میں بڑھا دیتے ہیں یا دو گروپوں کو نزدیک کے ایٹم سے نکالنے کے ل a ڈبل بانڈ بناتے ہیں۔ یہ ہائیڈروولیس کی طرح کام کرتے ہیں ، سوائے اس کے کہ ہٹا ہوا جزو پانی یا پانی کے کچھ حصوں سے بے گھر نہیں ہوتا ہے۔ خامروں کی اس کلاس میں آکسیلیٹ ڈیکربوکسیلیسی اور آئسوکیٹریٹ لیز شامل ہیں۔
- آئیسومریسیس - یہ انزائم آئسومرائزیشن رد عمل کو تیز کرتے ہیں۔ یہ وہ ردtions عمل ہیں جن میں ری ایکٹنٹ میں موجود تمام اصل جوہری برقرار رہتے ہیں ، لیکن ری ایکٹنٹ کا ایک آئومر بنانے کے لئے ان کو دوبارہ ترتیب دیا جاتا ہے۔ آئیسومرز ایک ہی کیمیائی فارمولے کے ساتھ مالیکیول ہیں ، لیکن مختلف انتظامات۔ مثالوں میں گلوکوز فاسفیٹ آئومومیراز اور الانائن ریسسمیس شامل ہیں۔
- لیگیسس - جسے مصنوعاتی غذا بھی کہا جاتا ہے ، یہ انزائم دو مالیکیولوں میں شامل ہونے کی شرح میں اضافہ کرتے ہیں۔ وہ عام طور پر اڈینوسین ٹرائفوسفیٹ (اے ٹی پی) کی خرابی سے حاصل ہونے والی توانائی کا استعمال کرکے یہ کام انجام دیتے ہیں۔ ligases کی مثالوں میں Acetyl-CoA synthetase اور DNA ligase شامل ہیں۔

