Kuna sheria tatu za kimsingi za gesi (Sheria ya Boyle, Sheria ya Charles, na Sheria ya Avogadro) ambayo inaelezea uhusiano wa shinikizo, joto, kiasi na kiasi cha gesi. Katika somo hili, tutajadili yafuatayo
Imetajwa baada ya Robert Boyle.
Hii inasema kwamba kiasi ni kinyume na shinikizo wakati halijoto na idadi ya molekuli ni mara kwa mara.
\(P ∝ 1/V\)
\(P = k_1V\)
wapi,
P ni shinikizo
V ni kiasi
na, k 1 ni uwiano thabiti
Sasa, ikiwa molekuli ya kudumu ya gesi hupata upanuzi kwa joto la mara kwa mara basi kiasi cha mwisho na shinikizo itakuwa P 2 na V 2 .
Kiasi cha awali na shinikizo la awali hapa ni P 1 na V 1 , basi kulingana na sheria ya Boyle:
\(P_1 \times V_1 = P_2 \times V_2 =constant (k_1) \)
\(or,\frac{P_1}{P_2} = \frac{V_2}{V_1} \)
Kwa hiyo, kwa joto la mara kwa mara, ikiwa shinikizo limeongezeka mara mbili, kiasi cha gesi hiyo kinapungua hadi nusu. Katika hali ya bure, dutu ya gesi inachukua kiasi kikubwa cha chombo kutokana na molekuli zilizotawanyika. Wakati shinikizo linatumika kwa dutu ya gesi, molekuli hizi huja karibu na kuchukua kiasi kidogo. Kwa maneno mengine, shinikizo lililowekwa ni sawia moja kwa moja na wiani wa gesi.
Hapa kuna uwakilishi wa picha wa Sheria ya Boyle:
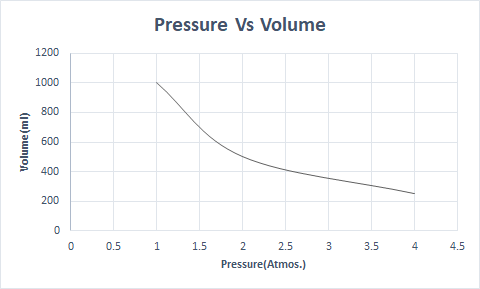
Katika mwinuko wa juu, shinikizo la anga ni la chini kwa hivyo hewa haina mnene. Matokeo yake, oksijeni kidogo inapatikana kwa kupumua. Hii ndiyo sababu wapanda milima hubeba mitungi ya oksijeni.
Mnamo 1787, Jacques Charles alisoma athari ya joto kwenye kiasi cha dutu ya gesi kwa shinikizo la mara kwa mara. Sheria ya Charles inasema kwamba kwa shinikizo la mara kwa mara na wingi wa mara kwa mara, kiasi cha gesi kinalingana moja kwa moja na joto.
\(V ∝ T\)
\(V = yT\)
Ambapo y ni mara kwa mara kulingana na kiasi cha gesi na shinikizo.
Sheria ya Charles imeonyeshwa kama:
\(\frac{V_1}{T_1} = \frac{V_2}{T_2}\)
Hii ina maana kwamba kwa ongezeko la joto kiasi kitaongezeka; kwa kupungua kwa joto, kiasi hupungua. Katika jaribio lake, alihesabu kwamba kiasi cha molekuli fulani ya gesi huongezeka au hupungua kwa mara 1/273.15 ya kiasi cha awali na kila digrii kupanda au kushuka kwa joto kwa mtiririko huo.
Kwa hivyo, ikiwa sauti ni V 0 kwa 0 O C na V t ni sauti ya t o C basi,
\(V_t = V_0 + \frac{t}{273.15} V_0\)
Huu hapa ni uwakilishi wa picha wa Sheria ya Charles:
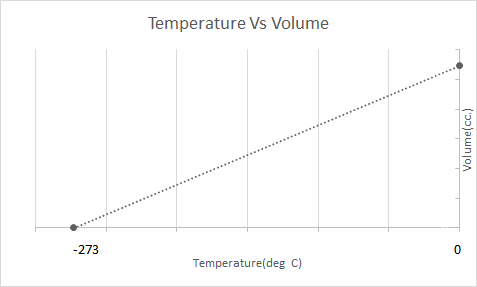
Puto za hewa moto hufanya kazi kwa misingi ya Sheria ya Charles. Wakati burner inapokanzwa hewa iliyonaswa ndani ya puto, molekuli za hewa huanza kusonga kwa kasi na kupanua. Gesi ndani ya puto inachukua nafasi zaidi, inakuwa chini ya mnene kuliko hewa inayoizunguka. Kadiri puto ya hewa moto inavyopungua, huinuka na kuelea.
Hii pia inajulikana kama Sheria ya Shinikizo. Iliundwa na Joseph Louis Gay-Lussac mnamo 1808.
Sheria ya Gay Lussac inasema kwamba kwa kiasi cha mara kwa mara, shinikizo la gesi bora ni sawia moja kwa moja na joto lake kamili (katika Kelvin).
\(P ∝ T\)
\(P/T = k \)
wapi
Sheria ya Gay-Lussac inaweza kuonyeshwa kama:
\(\frac{P_1}{T_1} = \frac{P_2}{T_2}\)
Wapi:
Kulingana na Sheria ya Gay-Lussac, mgandamizo wa gesi (iliyowekwa kwa kiwango kisichobadilika) hupungua mara kwa mara inapopozwa hadi hatimaye gesi hupitia ufupisho na kuwa kioevu.
Huu hapa ni uwakilishi wa picha wa Sheria ya Mashoga-Lussac
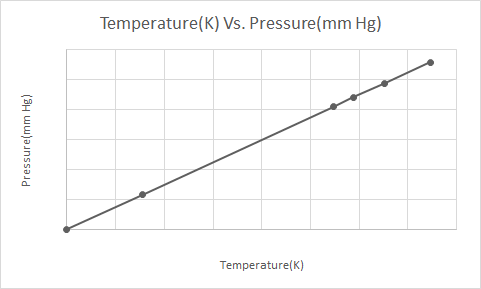
Wakati kopo la erosoli iliyoshinikizwa (km deodorant au kopo la rangi ya kunyunyuzia) linapokanzwa, ongezeko linalotokana na shinikizo linalotolewa na gesi kwenye chombo linaweza kusababisha mlipuko. Hii ndiyo sababu vyombo vingi vilivyoshinikizwa vina lebo za onyo zinazosema kwamba chombo lazima kiwekwe mbali na moto na kuhifadhiwa katika mazingira ya baridi.
Wakati jiko la shinikizo linapokanzwa, shinikizo la mvuke ndani ya chombo huongezeka. Joto la juu na shinikizo ndani ya chombo husababisha chakula kupika haraka.