आप सीखेंगे :
एक अणु दो या दो से अधिक परमाणुओं का एक समूह है जो रासायनिक रूप से एक साथ जुड़ते हैं। उदाहरण के लिए, हाइड्रोजन के दो परमाणु मिलकर हाइड्रोजन का एक अणु बनाते हैं। इसी तरह, सोडियम का एक परमाणु क्लोरीन के एक परमाणु के साथ मिलकर सोडियम क्लोराइड का एक अणु बनाता है। हम यह भी कह सकते हैं, अणु किसी तत्व या यौगिक का सबसे छोटा कण है जो स्वतंत्र अस्तित्व में सक्षम है और उस तत्व या यौगिक के सभी गुणों को दर्शाता है।
हम अणुओं को तत्वों के अणुओं और यौगिकों के अणुओं में विभाजित कर सकते हैं।
किसी तत्व के अणु एक ही प्रकार के परमाणुओं से बने होते हैं। हीलियम (He) जैसे कुछ तत्वों के अणु उस तत्व के केवल एक परमाणु से बने होते हैं। लेकिन ऑक्सीजन, नाइट्रोजन आदि तत्वों के परमाणु स्वतंत्र रूप से मौजूद नहीं हो सकते।
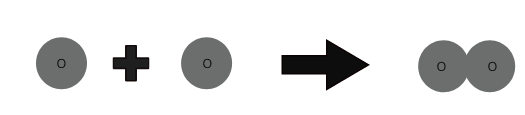
1 ऑक्सीजन परमाणु + 1 ऑक्सीजन परमाणु ⇒ 1 ऑक्सीजन अणु
किसी तत्व के अणु में उपस्थित परमाणुओं की संख्या उसकी परमाणुता कहलाती है। परमाणु एक परमाणु , द्विपरमाणुक, त्रिपरमाणुक और बहुपरमाणुक हो सकता है।
| परमाणुता | परमाणुओं की संख्या | उदाहरण |
| एकपरमाणुक | 1 | हीलियम ( \(He\) ), नियॉन ( \(Ne\) ) जैसी महान गैसें |
| दो परमाणुओंवाला | 2 | हाइड्रोजन ( \(H_2\) ) क्लोरीन ( \(Cl_2\) ) |
| त्रिपरमाण्विक | 3 | ओजोन ( \(O_3\) ) |
| बहुपरमाणुक | > 2 | फास्फोरस ( \(P_4\) ) परमाणु 4 सल्फर ( \(S_8\) ) परमाणु 8 |
एक रासायनिक यौगिक एक रासायनिक पदार्थ को संदर्भित करता है जो कई समान अणुओं से बना होता है जो एक से अधिक तत्वों के परमाणुओं से बने होते हैं जो रासायनिक बंधों से जुड़े होते हैं। अणु में बंधे एक ही तत्व से दो परमाणु रासायनिक यौगिक नहीं बनाते हैं, ऐसा इसलिए है क्योंकि इसके लिए दो अलग-अलग तत्वों की आवश्यकता होती है।
प्रकृति में पाए जाने वाले अधिकांश पदार्थ - जैसे लकड़ी, मिट्टी और चट्टानें - रासायनिक यौगिकों के मिश्रण हैं।
एक यौगिक की एक परिभाषित विशेषता यह है कि इसका एक रासायनिक सूत्र होता है। सूत्र किसी पदार्थ में परमाणुओं के अनुपात का वर्णन करते हैं। उदाहरण के लिए, पानी के अणु का सूत्र एच 2 ओ है। यह इंगित करता है कि दो हाइड्रोजन परमाणु एक ऑक्सीजन परमाणु से बंधे होते हैं।
विभिन्न तत्वों के परमाणु एक निश्चित अनुपात में एक साथ मिलकर यौगिकों के अणु बनाते हैं। उदाहरण के लिए, पानी ( \(H_2O\) ) मिश्रित पानी के एक अणु का प्रतिनिधित्व करता है जिसमें हाइड्रोजन के दो परमाणु ऑक्सीजन के एक परमाणु के साथ जुड़ते हैं।
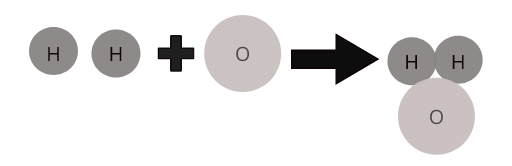
कुछ सामान्य यौगिकों के अणु:
| मिश्रण | तत्वों का संयोजन |
| हाइड्रोजन क्लोराइड ( \(HCl\) ) | हाइड्रोजन, क्लोरीन |
| पानी ( \(H_2O\) ) | हाइड्रोजन, ऑक्सीजन |
| कार्बन डाइऑक्साइड ( \(CO_2\) ) | कार्बन, ऑक्सीजन |
जब परमाणु एक-दूसरे के करीब आते हैं, तो वे मिलकर अणु बनाते हैं। जब वे संयुक्त होते हैं, तो एक परमाणु एक या एक से अधिक इलेक्ट्रॉन देता है या दान करता है जिसे अन्य परमाणुओं द्वारा स्वीकार किया जाता है। नतीजतन, एक रासायनिक बंधन बनता है जो एक यौगिक बनाने के लिए परमाणुओं को एक साथ रखता है।
संयोजकता इलेक्ट्रॉनों की संख्या है जिसे एक परमाणु किसी अन्य परमाणु के साथ एक रासायनिक यौगिक या अणु बनाने के लिए निरूपित या स्वीकार कर सकता है। यह किसी तत्व के परमाणु की संयोजन क्षमता है।
संयोजकता हमेशा एक पूर्ण संख्या होती है। संयोजकता 1 वाले तत्व मोनोवैलेंट कहलाते हैं । संयोजकता 2 वाले तत्व द्विसंयोजी तथा 3 के बराबर संयोजकता त्रिसंयोजक कहलाते हैं। कई तत्वों में परिवर्तनशील संयोजकता (एक से अधिक संयोजकता) होती है। एक से अधिक संयोजकता वाले तत्व को उस तत्व के नाम के रूप में लिखा जाता है जिसके बाद कोष्ठक में रोमन अंक द्वारा संयोजकता को दर्शाया जाता है। उदाहरण के लिए, संयोजकता 1 वाले तांबे को कॉपर [I] के रूप में लिखा जाता है।
कुछ तत्व और उनकी संयोजकता:
| तत्व | संयोजकता |
| हाइड्रोजन ( \(H\) ) | 1 |
| हीलियम ( \(He\) ) | 0 |
| कार्बन ( \(C\) ) | 4 |
| नाइट्रोजन ( \(N\) ) | 3 |
| ऑक्सीजन ( \(O\) ) | 2 |
| सोडियम ( \(Na\) ) | 1 |
| मैग्नीशियम ( \(Mg\) ) | 2 |
| फास्फोरस ( \(P\) ) | 3 |
| सल्फर ( \(S\) ) | 2 |
| क्लोरीन ( \(Cl\) ) | 1 |
| पोटेशियम ( \(K\) ) | 1 |
| कैल्शियम ( \(Ca\) ) | 2 |
| कॉपर ( \(Cu\) ) | 1 2 |
| आयरन ( \(Fe\) ) | 2 3 |
किसी यौगिक का रासायनिक सूत्र उसकी संरचना का प्रतीकात्मक निरूपण है। यह हमें एक यौगिक के एक अणु में मौजूद विभिन्न तत्वों के परमाणुओं की संख्या बताता है।
यौगिक का सूत्र लिखने के नियम:
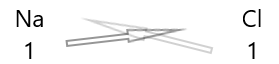
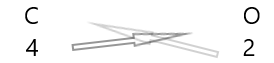
1 . तत्वों के प्रतीक और उनके नीचे उनकी संयोजकता लिखिए।
2. उनकी संयोजकता को आपस में बदलें और उन्हें सबस्क्रिप्ट के रूप में लिखें।
3. यदि रासायनिक सूत्र में संयोजकताएँ किसी गुणनखंड से विभाज्य हैं, तो विभाजित और सरल कीजिए।
रासायनिक यौगिक विशेषताओं की एक चौंकाने वाली सरणी दिखाते हैं। सामान्य तापमान और दबाव पर, कुछ ठोस होते हैं, कुछ तरल होते हैं और कुछ गैस होते हैं। रासायनिक यौगिक विविध रंगों के होते हैं। कुछ यौगिक मनुष्यों के लिए अत्यधिक विषैले होते हैं, जबकि अन्य जीवन के लिए आवश्यक होते हैं। किसी यौगिक के भीतर केवल एक परमाणु का प्रतिस्थापन किसी पदार्थ के रंग, गंध या विषाक्तता को बदलने के लिए जिम्मेदार हो सकता है।