Imparerai :
Una molecola è un gruppo di due o più atomi uniti chimicamente. Ad esempio, due atomi di idrogeno si combinano per formare una molecola di idrogeno. Allo stesso modo, un atomo di sodio si combina con un atomo di cloro per formare una molecola di cloruro di sodio. Possiamo anche dire che una molecola è la particella più piccola di un elemento o di un composto che è capace di esistere in modo indipendente e mostra tutte le proprietà di quell'elemento o composto.
Possiamo dividere le molecole in molecole di elementi e molecole di composti .
Le molecole di un elemento sono costituite dallo stesso tipo di atomi. Le molecole di alcuni elementi come l'elio (He) sono costituite da un solo atomo di quell'elemento. Ma gli atomi di elementi come ossigeno, azoto, ecc. non possono esistere indipendentemente.
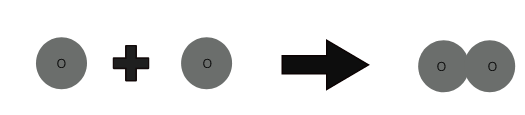
1 atomo di ossigeno + 1 atomo di ossigeno ⇒ 1 molecola di ossigeno
Il numero di atomi presenti in una molecola di un elemento è chiamato la sua atomicità. L'atomicità può essere monoatomica, biatomica, triatomica e poliatomica.
| Atomicita | Numero di atomi | Esempi |
| Monoatomico | 1 | Gas nobili come Elio( \(He\) ), Neon( \(Ne\) ) |
| Biatomico | 2 | Idrogeno( \(H_2\) ) Cloro( \(Cl_2\) ) |
| Triatomico | 3 | Ozono( \(O_3\) ) |
| Poliatomico | > 2 | Fosforo( \(P_4\) ) Atomicità 4 Zolfo( \(S_8\) ) Atomicità 8 |
Un composto chimico si riferisce a una sostanza chimica composta da molte molecole identiche composte da atomi di più di un elemento uniti insieme da legami chimici. Due atomi dello stesso elemento legati in una molecola non formano un composto chimico, questo perché questo richiede due elementi diversi.
La maggior parte delle sostanze presenti in natura, come legno, terra e rocce, sono miscele di composti chimici.
Una caratteristica distintiva di un composto è che ha una formula chimica. Le formule descrivono il rapporto tra gli atomi in una sostanza. Ad esempio, la formula di una molecola d'acqua è H 2 O. questo indica che due atomi di idrogeno sono legati a un atomo di ossigeno.
Gli atomi di diversi elementi si combinano insieme in una proporzione definita per formare molecole di composti. Ad esempio, l'acqua ( \(H_2O\) ) rappresenta una molecola del composto acqua in cui due atomi di idrogeno si combinano con un atomo di ossigeno.
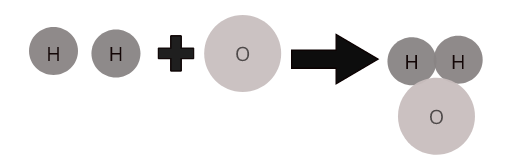
Molecole di alcuni composti comuni:
| Composto | Combinazione di elementi |
| Cloruro di idrogeno ( \(HCl\) ) | Idrogeno, Cloro |
| Acqua ( \(H_2O\) ) | Idrogeno, Ossigeno |
| Anidride carbonica ( \(CO_2\) ) | Carbonio, Ossigeno |
Quando gli atomi si avvicinano gli uni agli altri, si combinano per formare molecole. Quando si combinano, un atomo dà o dona uno o più elettroni che viene accettato dagli altri atomi. Di conseguenza, si forma un legame chimico che tiene insieme gli atomi per formare un composto.
La valenza è il numero di elettroni che un atomo può denotare o accettare per formare un composto chimico o molecole con un altro atomo. È la capacità combinante di un atomo di un elemento.
Una valenza è sempre un numero intero. Gli elementi con valenza 1 sono detti monovalenti. Gli elementi con valenza 2 sono detti bivalenti e quelli con valenza uguale a 3 sono detti trivalenti. Molti elementi hanno valenza variabile (più di una valenza). Un elemento con più di una valenza è scritto come il nome dell'elemento seguito da un numero romano tra parentesi per indicare la valenza. Ad esempio, il rame con valenza 1 è scritto come Copper[I]
Pochi elementi e la loro valenza:
| Elemento | Valenza |
| Idrogeno ( \(H\) ) | 1 |
| Elio( \(He\) ) | 0 |
| Carbonio( \(C\) ) | 4 |
| Azoto( \(N\) ) | 3 |
| Ossigeno( \(O\) ) | 2 |
| Sodio( \(Na\) ) | 1 |
| Magnesio( \(Mg\) ) | 2 |
| Fosforo( \(P\) ) | 3 |
| Zolfo( \(S\) ) | 2 |
| Cloro( \(Cl\) ) | 1 |
| Potassio( \(K\) ) | 1 |
| Calcio( \(Ca\) ) | 2 |
| Rame( \(Cu\) ) | 1 2 |
| Ferro( \(Fe\) ) | 2 3 |
La formula chimica di un composto è la rappresentazione simbolica della sua composizione. Ci dice il numero di atomi di vari elementi presenti in una molecola di un composto.
Regole per scrivere la formula di un composto:
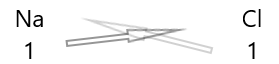
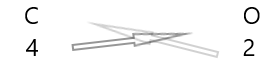
1 . Scrivi sotto di essi il simbolo degli elementi e la loro valenza.
2. Scambia la loro valenza e scrivili come pedici.
3. Se le valenze nella formula chimica sono divisibili per qualsiasi fattore, dividi e semplifica.
I composti chimici mostrano una gamma sconcertante di caratteristiche. A temperature e pressioni ordinarie, alcuni sono solidi, altri sono liquidi e altri sono gas. I composti chimici sono di vari colori. Alcuni composti sono altamente tossici per l'uomo, mentre altri sono essenziali per la vita. La sostituzione di un solo atomo all'interno di un composto può essere responsabile del cambiamento del colore, dell'odore o della tossicità di una sostanza.