Dowiesz się :
Cząsteczka to grupa dwóch lub więcej atomów, które są ze sobą połączone chemicznie. Na przykład dwa atomy wodoru łączą się, tworząc cząsteczkę wodoru. Podobnie jeden atom sodu łączy się z jednym atomem chloru, tworząc cząsteczkę chlorku sodu. Można też powiedzieć, że cząsteczka to najmniejsza cząsteczka pierwiastka lub związku, która jest zdolna do niezależnego istnienia i wykazuje wszystkie właściwości tego pierwiastka lub związku.
Cząsteczki możemy podzielić na cząsteczki pierwiastków i cząsteczki związków .
Cząsteczki pierwiastka zbudowane są z tego samego rodzaju atomów. Cząsteczki niektórych pierwiastków takich jak hel (He) składają się tylko z jednego atomu tego pierwiastka. Ale atomy pierwiastków, takich jak tlen, azot itp., Nie mogą istnieć niezależnie.
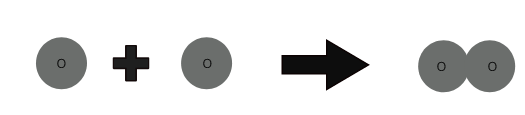
1 atom tlenu + 1 atom tlenu ⇒ 1 cząsteczka tlenu
Liczba atomów obecnych w cząsteczce pierwiastka nazywana jest jego atomowością. Atomowość może być jednoatomowa, dwuatomowa, trójatomowa i wieloatomowa.
| Atomowość | Liczba atomów | Przykłady |
| Monoatomowy | 1 | Gazy szlachetne, takie jak hel( \(He\) ), neon( \(Ne\) ) |
| Dwuatomowy | 2 | Wodór( \(H_2\) ) Chlor( \(Cl_2\) ) |
| Trójatomowy | 3 | Ozon( \(O_3\) ) |
| Wieloatomowy | > 2 | Fosfor( \(P_4\) ) Atomowość 4 Siarka( \(S_8\) ) Atomowość 8 |
Związek chemiczny odnosi się do substancji chemicznej, która składa się z wielu identycznych cząsteczek, które składają się z atomów z więcej niż jednego pierwiastka połączonych ze sobą wiązaniami chemicznymi. Dwa atomy z tego samego pierwiastka związane w cząsteczce nie tworzą związku chemicznego, ponieważ wymaga to dwóch różnych pierwiastków.
Większość substancji występujących w przyrodzie – takich jak drewno, gleba i skały – to mieszaniny związków chemicznych.
Charakterystyczną cechą związku jest to, że ma on wzór chemiczny. Wzory opisują stosunek atomów w substancji. Na przykład wzór cząsteczki wody to H2O . Oznacza to, że dwa atomy wodoru są związane z jednym atomem tlenu.
Atomy różnych pierwiastków łączą się ze sobą w określonej proporcji, tworząc cząsteczki związków. Na przykład woda ( \(H_2O\) ) reprezentuje cząsteczkę wody złożonej, w której dwa atomy wodoru łączą się z jednym atomem tlenu.
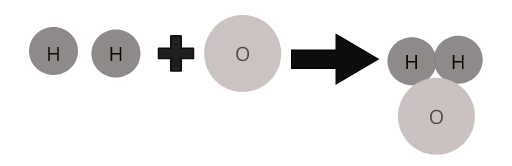
Cząsteczki niektórych typowych związków:
| Mieszanina | Łączenie elementów |
| Chlorowodór ( \(HCl\) ) | wodór, chlor |
| Woda ( \(H_2O\) ) | Wodór, tlen |
| Dwutlenek węgla ( \(CO_2\) ) | węgiel, tlen |
Kiedy atomy zbliżają się do siebie, łączą się, tworząc cząsteczki. Kiedy się łączą, jeden atom daje lub przekazuje jeden lub więcej elektronów, które są akceptowane przez inne atomy. W rezultacie powstaje wiązanie chemiczne, które łączy atomy, tworząc związek.
Wartościowość to liczba elektronów, które atom może oznaczyć lub zaakceptować, tworząc związek chemiczny lub cząsteczki z innym atomem. Jest to zdolność łączenia atomu pierwiastka.
Wartościowość jest zawsze liczbą całkowitą. Pierwiastki o wartościowości 1 nazywane są jednowartościowymi. Pierwiastki o wartościowości 2 nazywane są dwuwartościowymi , a wartościowości równej 3 trójwartościowymi. Wiele pierwiastków ma zmienną wartościowość (więcej niż jedną wartościowość). Pierwiastek z więcej niż jedną wartościowością jest zapisywany jako nazwa pierwiastka, po której następuje cyfra rzymska w nawiasach wskazująca wartościowość. Na przykład miedź o wartościowości 1 jest zapisywana jako miedź [I]
Kilka pierwiastków i ich wartościowość:
| Element | Wartościowość |
| Wodór ( \(H\) ) | 1 |
| Hel( \(He\) ) | 0 |
| Węgiel( \(C\) ) | 4 |
| Azot( \(N\) ) | 3 |
| tlen( \(O\) ) | 2 |
| Sód( \(Na\) ) | 1 |
| Magnez( \(Mg\) ) | 2 |
| Fosfor( \(P\) ) | 3 |
| Siarka( \(S\) ) | 2 |
| Chlor( \(Cl\) ) | 1 |
| Potas( \(K\) ) | 1 |
| Wapń( \(Ca\) ) | 2 |
| Miedź( \(Cu\) ) | 1 2 |
| Żelazo( \(Fe\) ) | 2 3 |
Wzór chemiczny związku jest symbolicznym przedstawieniem jego składu. Mówi nam o liczbie atomów różnych pierwiastków obecnych w jednej cząsteczce związku.
Zasady pisania wzoru związku:
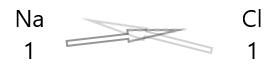
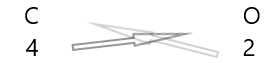
1 . Wpisz pod nimi symbole pierwiastków i ich wartościowość.
2. Zamień ich wartościowości i zapisz je jako indeksy dolne.
3. Jeśli wartościowości we wzorze chemicznym są podzielne przez jakikolwiek czynnik, podziel i uprość.
Związki chemiczne wykazują zdumiewający wachlarz właściwości. W zwykłych temperaturach i ciśnieniach niektóre są ciałami stałymi, niektóre cieczami, a niektóre gazami. Związki chemiczne mają różne kolory. Niektóre związki są wysoce toksyczne dla ludzi, podczas gdy inne są niezbędne do życia. Zastąpienie tylko jednego atomu w związku może być odpowiedzialne za zmianę koloru, zapachu lub toksyczności substancji.