آپ سیکھیں گے :
ایک مالیکیول دو یا دو سے زیادہ ایٹموں کا ایک گروپ ہے جو کیمیائی طور پر آپس میں جڑے ہوئے ہیں۔ مثال کے طور پر، ہائیڈروجن کے دو ایٹم مل کر ہائیڈروجن کا مالیکیول بناتے ہیں۔ اسی طرح، سوڈیم کا ایک ایٹم کلورین کے ایک ایٹم کے ساتھ مل کر سوڈیم کلورائد کا مالیکیول بناتا ہے۔ ہم یہ بھی کہہ سکتے ہیں کہ مالیکیول کسی عنصر یا مرکب کا سب سے چھوٹا ذرہ ہوتا ہے جو آزاد وجود کے قابل ہوتا ہے اور اس عنصر یا مرکب کی تمام خصوصیات کو ظاہر کرتا ہے۔
ہم انووں کو عناصر کے مالیکیولز اور مرکبات کے مالیکیولز میں تقسیم کر سکتے ہیں۔
ایک عنصر کے مالیکیول ایک ہی قسم کے ایٹموں سے بنے ہوتے ہیں۔ کچھ عناصر جیسے ہیلیم (He) کے مالیکیول اس عنصر کے صرف ایک ایٹم سے بنتے ہیں۔ لیکن آکسیجن، نائٹروجن وغیرہ جیسے عناصر کے ایٹم آزادانہ طور پر موجود نہیں ہو سکتے۔
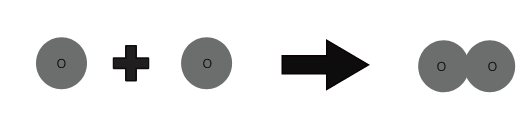
1 آکسیجن ایٹم + 1 آکسیجن ایٹم ⇒ 1 آکسیجن مالیکیول
کسی عنصر کے مالیکیول میں موجود ایٹموں کی تعداد کو اس کی ایٹمیسیٹی کہتے ہیں۔ جوہری ایک ایٹمی، ڈائیٹومک، ٹرائیاٹومک اور پولیٹومک ہوسکتا ہے۔
| جوہری | ایٹموں کی تعداد | مثالیں |
| یک ایٹمی | 1 | نوبل گیسیں جیسے ہیلیم ( \(He\) )، نیین ( \(Ne\) ) |
| ڈائیٹومک | 2 | ہائیڈروجن ( \(H_2\) ) کلورین ( \(Cl_2\) ) |
| ٹرائیاٹومک | 3 | اوزون ( \(O_3\) ) |
| پولیٹومک | > 2 | فاسفورس ( \(P_4\) ) جوہری 4 سلفر( \(S_8\) ) جوہری 8 |
کیمیائی مرکب سے مراد ایک کیمیائی مادہ ہے جو بہت سے ایک جیسے مالیکیولز پر مشتمل ہوتا ہے جو ایک سے زیادہ عناصر کے ایٹموں پر مشتمل ہوتے ہیں جو کیمیکل بانڈز کے ذریعے آپس میں جڑے ہوتے ہیں۔ مالیکیول میں جڑے ایک ہی عنصر سے دو ایٹم ایک کیمیائی مرکب نہیں بناتے، اس کی وجہ یہ ہے کہ اس کے لیے دو مختلف عناصر کی ضرورت ہوتی ہے۔
فطرت میں پائے جانے والے زیادہ تر مادے - جیسے لکڑی، مٹی اور چٹانیں - کیمیائی مرکبات کا مرکب ہیں۔
ایک مرکب کی ایک وضاحتی خصوصیت یہ ہے کہ اس کا ایک کیمیائی فارمولا ہے۔ فارمولے کسی مادہ میں ایٹموں کے تناسب کو بیان کرتے ہیں۔ مثال کے طور پر، پانی کے مالیکیول کا فارمولا H 2 O ہے۔ یہ بتاتا ہے کہ دو ہائیڈروجن ایٹم ایک آکسیجن ایٹم سے جڑے ہوئے ہیں۔
مختلف عناصر کے ایٹم ایک خاص تناسب میں مل کر مرکبات کے مالیکیول بناتے ہیں۔ مثال کے طور پر، پانی ( \(H_2O\) ) مرکب پانی کے ایک مالیکیول کی نمائندگی کرتا ہے جس میں ہائیڈروجن کے دو ایٹم آکسیجن کے ایک ایٹم کے ساتھ مل جاتے ہیں۔
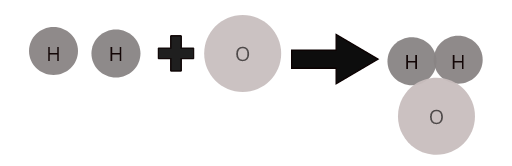
کچھ عام مرکبات کے مالیکیولز:
| کمپاؤنڈ | عناصر کا امتزاج |
| ہائیڈروجن کلورائیڈ ( \(HCl\) ) | ہائیڈروجن، کلورین |
| پانی ( \(H_2O\) ) | ہائیڈروجن، آکسیجن |
| کاربن ڈائی آکسائیڈ ( \(CO_2\) ) | کاربن، آکسیجن |
جب ایٹم ایک دوسرے کے قریب آتے ہیں تو وہ مل کر مالیکیول بناتے ہیں۔ جب وہ یکجا ہوتے ہیں تو ایک ایٹم ایک یا زیادہ الیکٹران دیتا ہے یا عطیہ کرتا ہے جسے دوسرے ایٹم قبول کرتے ہیں۔ نتیجے کے طور پر، ایک کیمیائی بانڈ تشکیل دیا جاتا ہے جو ایک مرکب بنانے کے لئے ایٹموں کو ایک ساتھ رکھتا ہے.
ویلنسی الیکٹرانوں کی وہ تعداد ہے جسے ایک ایٹم کسی دوسرے ایٹم کے ساتھ کیمیائی مرکب یا مالیکیول بنانے کے لیے ظاہر یا قبول کر سکتا ہے۔ یہ ایک عنصر کے ایٹم کی یکجا کرنے کی صلاحیت ہے۔
ایک والینسی ہمیشہ ایک مکمل نمبر ہوتی ہے۔ valency 1 والے عناصر کو monovalent کہا جاتا ہے۔ valency 2 والے عناصر کو divalent کہا جاتا ہے اور 3 کے برابر valency کو trivalent کہا جاتا ہے۔ بہت سے عناصر میں متغیر والینسی ہوتی ہے (ایک سے زیادہ والینسی)۔ ایک سے زیادہ والینسی والے عنصر کو عنصر کے نام کے طور پر لکھا جاتا ہے جس کے بعد بریکٹ میں ایک رومن ہندسہ ہوتا ہے تاکہ valency کی نشاندہی کی جا سکے۔ مثال کے طور پر، والینسی 1 کے ساتھ تانبے کو Copper[I] کے طور پر لکھا جاتا ہے۔
چند عناصر اور ان کی ہم آہنگی:
| عنصر | ویلنسی |
| ہائیڈروجن ( \(H\) ) | 1 |
| ہیلیم ( \(He\) ) | 0 |
| کاربن ( \(C\) ) | 4 |
| نائٹروجن ( \(N\) ) | 3 |
| آکسیجن ( \(O\) ) | 2 |
| سوڈیم ( \(Na\) ) | 1 |
| میگنیشیم ( \(Mg\) ) | 2 |
| فاسفورس ( \(P\) ) | 3 |
| سلفر ( \(S\) ) | 2 |
| کلورین ( \(Cl\) ) | 1 |
| پوٹاشیم ( \(K\) ) | 1 |
| کیلشیم ( \(Ca\) ) | 2 |
| تانبا ( \(Cu\) ) | 1 2 |
| آئرن( \(Fe\) ) | 2 3 |
ایک مرکب کا کیمیائی فارمولا اس کی ساخت کی علامتی نمائندگی ہے۔ یہ ہمیں ایک مرکب کے ایک مالیکیول میں موجود مختلف عناصر کے ایٹموں کی تعداد بتاتا ہے۔
کمپاؤنڈ کا فارمولا لکھنے کے اصول:
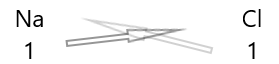
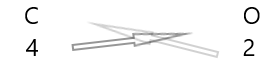
1 . عناصر کی علامت اور ان کے نیچے ان کی valency لکھیں۔
2. ان کی valency کا تبادلہ کریں اور انہیں بطور سبسکرپٹ لکھیں۔
3. اگر کیمیائی فارمولے میں valencies کسی بھی عنصر سے قابل تقسیم ہیں تو تقسیم کریں اور آسان کریں۔
کیمیائی مرکبات خصوصیات کی ایک حیران کن صف دکھاتے ہیں۔ عام درجہ حرارت اور دباؤ میں، کچھ ٹھوس، کچھ مائع اور کچھ گیسیں ہیں۔ کیمیائی مرکبات مختلف رنگوں کے ہوتے ہیں۔ کچھ مرکبات انسانوں کے لیے انتہائی زہریلے ہیں، جب کہ دیگر زندگی کے لیے ضروری ہیں۔ کسی مرکب کے اندر صرف ایک ایٹم کا متبادل مادہ کے رنگ، بدبو، یا زہریلے پن کے لیے ذمہ دار ہو سکتا ہے۔